Lexikon der Biologie: phototrophe Bakterien
phototrophe Bakterien [von *photo- , griech. trophē = Ernährung], photosynthetische Bakterien, 1) i.w.S. alle prokaryotischen Mikroorganismen, die Licht-Energie als Energiequelle nutzen, Cyanobakterien (einschließlich der Prochlorales), Anoxyphotobacteria (anoxygene phototrophe Bakterien, s.u.) und Halobakterien (Archaebakterien). 2) i.e.S. die Anoxyphotobacteria, Bakterien, die Licht in einer anoxygenen Photosynthese als Energiequelle zum Wachstum nutzen. Sie besitzen nur 1 Photosystem, PS I oder II (Photosynthese), und können daher, im Gegensatz zu grünen Pflanzen und Cyanobakterien, Wasser nicht als Wasserstoffdonor (Wasserstoff) zur Kohlendioxidassimilation verwerten, sondern sind auf stärker reduzierte Verbindungen, z.B. H2S (Schwefelwasserstoff), H2, Eisen-II-Verbindungen oder einfache organische Stoffe, angewiesen; folglich wird kein O2 (Sauerstoff) entwickelt. Phototrophe Bakterien sind typische Wasserbakterien in Süß-, Brack- und Salzwasser sowie feuchten Böden und überfluteten Feldern; beweglich oder unbeweglich, grün, gelblich, braun oder rötlich (purpur) gefärbt; viele enthalten Gasvakuolen (z.B. Lamprocystis, Thiodictyon, Pelodictyon, Ancalochloris). Bei einigen Gruppen, besonders unter Bedingungen, wo Licht einfällt und organische Stoffe unter sauerstofffreien oder -limitierten Bedingungen abgebaut werden, kann eine grünliche oder rötliche Wasserblüte auftreten. Schwefelverwertende phototrophe Bakterien leben oft in enger Stoffwechselgemeinschaft mit chemoorganotrophen Sulfatreduzierern und Schwefelreduzierern (Consortium); sie spielen in der Natur eine zentrale Rolle im biochemischen Schwefelkreislauf. Große Bedeutung haben phototrophe Bakterien in der Kohlendioxidassimilation unterhalb der Oberfläche meromiktischer Seen (20–85% der Gesamt-Tagesproduktion) als Nahrungsquelle für Zoo-Plankton und zur gleichzeitigen Beseitigung des toxischen Schwefelwasserstoffs aus dem Faulschlamm ( vgl. Abb. 1 ). Nach Pigmentzusammensetzung, morphologischen und physiologischen Merkmalen wurden früher in künstlichen praktischen Systemen 2 Gruppen, die grünen Bakterien und die Purpurbakterien, mit je 2 Familien unterschieden ( vgl. Tab. 1 ). Neuere molekulargenetische Untersuchungen (16S-rDNA ) ergaben jedoch, daß die anoxygenen phototrophen Bakterien zur Zeit 4 unterschiedlichen Abstammungslinien zuzuordnen sind, hauptsächlich Zweigen der Proteobacteria ( vgl. Tab. 2 ; Purpurbakterien). Einige gehören aber auch zu den grampositiven Bakterien mit niedrigem GC-Gehalt (Ordnung Clostridiales, vorläufige Familie Heliobacteriaceae), zur Zeit mit den Gattungen Heliobacterium, Heliophilum und Heliobacillus. Diese anaeroben Heliobakterien können zusätzlich zu ihrem phototrophen Wachstum auch durch Pyruvatgärung chemotroph wachsen und sind daher photoheterotroph. Weitere Merkmale sind eine gleitende Bewegung und das Vorhandensein von Bakteriochlorophyll g. Sie leben im Boden, insbesondere in tropischen Reisfeldböden. Die Endosporen der Heliobakterien enthalten wie diejenigen von ClostridienDipicolinsäure. – Phototrophe Bakterien haben verschiedene Zellformen: Kokken, lange und kurze Stäbchen, Spirillen, netz- und plattenförmige Aggregate sowie Consortien; die Größe beträgt 1–2 μm bis 3,5 × 50 μm. Typische Pigmente des phototrophen Stoffwechsels sind Bakteriochlorophylle und bestimmte Carotinoide. Die Pigmente sind bei den Purpurbakterien hauptsächlich in und an intracytoplasmatischen Membranen (Thylakoide, Chromatophoren) verschiedener Form lokalisiert ( vgl. Abb. 2 ); ihre Ausbildung ist von den Umweltbedingungen, besonders vom Sauerstoff-Partialdruck und der Lichtintensität, abhängig (Purpurbakterien). Bei den grünen Bakterien ist das Reaktionszentrum des phototrophen Energiegewinns in der Cytoplasmamembran lokalisiert, und die Antennenpigmente liegen auf besonderen Proteinstrukturen, den Chlorosomen. Es gibt auch phototrophe Bakterien ohne ausgeprägte innere Membranen und ohne Chlorosomen, z.B. Heliobacterium. Die grünen Schwefelbakterien und die Schwefelpurpurbakterien verwenden in der Photosynthese vorwiegend reduzierte Schwefelverbindungen, wie H2S ( vgl. Abb. 3 ), S°, S2O32–, zur Bildung von Reduktionsäquivalenten [NAD(P)H; Nicotinamidadenindinucleotid, Nicotinamidadenindinucleotidphosphat]. Die schwefelfreien Purpurbakterien benötigen in der Regel organische Substrate (Säuren, Zucker) für Reduktionen und als Kohlenstoffquelle. Sie können aber auch, wie die Vertreter der beiden anderen Familien, mit Wasserstoff und Kohlendioxid photolithoautotroph (Photolithotrophie) wachsen. Viele benötigen aber den Zusatz von Vitaminen. Die lichtabhängige ATP-Synthese (Adenosintriphosphat) der Phototrophen erfolgt über einen Protonengradienten (protonenmotorische Kraft), der durch einen lichtgetriebenen Elektronentransport aufgebaut wird. Bei den Purpurbakterien enthält der membrangebundene Photosyntheseapparat ( vgl. Abb. 4 ) 3–4 spezifische Komplexe, das Reaktionszentrum, meist 2 lichtsammelnde Antennenkomplexe (I und II) und den Cytochrom-bc1-Komplex (Cytochrome), der bei den fakultativ phototrophen Arten auch im Atmungsstoffwechsel funktionsfähig ist. Die dreidimensionale Struktur des Reaktionszentrums von Rhodopseudomonas viridis (= Blastochloris viridis), einem schwefelfreien Purpurbakterium, konnte mittels Röntgenstrukturanalyse bestimmt werden (J. Deisenhofer, R. Huber, H. Michel; Nobelpreis 1988). Das Photosystem der Purpurbakterien und von Chloroflexus aurantiacus ist dem Photosystem II und das der grünen Schwefelbakterien sowie der Heliobakterien dem Photosystem I der Cyanobakterien ähnlich. Im Photosystem II ist der terminale Elektronenakzeptor im Reaktionszentrum ein Schwefel-Eisen-Protein (Eisen-Schwefel-Proteine), im Photosystem I dagegen ein Chinon. Die Absorption der Reaktionszentrum-Chlorophylle (Bakteriochlorophylle [Abb.]) liegt bei den Purpurbakterien bei 870 nm (Bchl a) oder ca. 1020 nm (BChl b), bei den grünen Schwefelbakterien bei 840 nm (BChl a) ( vgl. Abb. 5 ) und bei den Heliobakterien 798 nm (BChl g). Die Kohlendioxidassimilation wird von den Purpurbakterien im Calvin-Zyklus, von den grünen Schwefelbakterien im reduktiven Citratzyklus durchgeführt. Die anoxygene Photosynthese findet überwiegend unter anaeroben Bedingungen statt, doch gibt es einige obligat aerobe Arten, die auch Bakteriochlorophyll enthalten (z.B. Roseobacter; vgl. Tab. 2 ). Während alle grünen und purpurfarbenen Schwefelbakterien einen obligaten (anaeroben) phototrophen Stoffwechsel besitzen, können einige Arten der schwefelfreien Purpurbakterien und der grünen, gleitenden phototrophen Bakterien fakultativ aerob im Dunkeln organische Substrate veratmen und wachsen. Im Atmungsstoffwechsel wird bei diesen fakultativen Phototrophen kein Photosyntheseapparat ausgebildet. Wenige Arten vermögen zusätzlich im Dunkeln bei Fehlen von Sauerstoff organische Stoffe zu vergären. Die meisten phototrophen Bakterien können anaerob im Licht molekularen Luft-Stickstoff fixieren. Bei einem Überschuß an Energie- und Reduktionskraft und einem Mangel an Stickstoffverbindungen (auch N2) entsteht über das Nitrogenase-System (Nitrogenase) H2, das zur „photobiologischen Wasserstoffbildung“ genutzt werden könnte. Proteine II .
G.S.
Lit.:Blankenship, R.E. et al. (eds:): Anoxygenic Photosynthetic Bacteria (Advances in Photosynthesis and Respiration; ed. Govindjee). 1995.

phototrophe Bakterien
Abb. 1: Verteilung phototropher Bakterien, Cyanobakterien und Algen in einem See. a) oxygene Phototrophe (Algen, Cyanobakterien); b) anoxygene Phototrophe (Schwefelpurpurbakterien, grüne Schwefelbakterien); c) Sediment mit chemoorganotrophen Gärern (Faulschlammbakterien).
ae = aerobe Zone mit gelöstem O2; an = anaerobe Zone ohne gelösten O2, aber mit gelöstem Schwefelwasserstoff (H2S) und CO2 aus dem Faulschlamm

phototrophe Bakterien
Abb. 2: Elektronenmikroskopische Aufnahme (Dünnschnitt) einer Zelle von Rhodopseudomonas capsulata (Rhodobacter capsulatus). Neben Poly-β-hydroxybuttersäure finden sich in den Zellen phototropher Bakterien noch Polysaccharide, Polyphosphate und bei Schwefelpurpurbakterien auch Schwefeleinschlüsse.
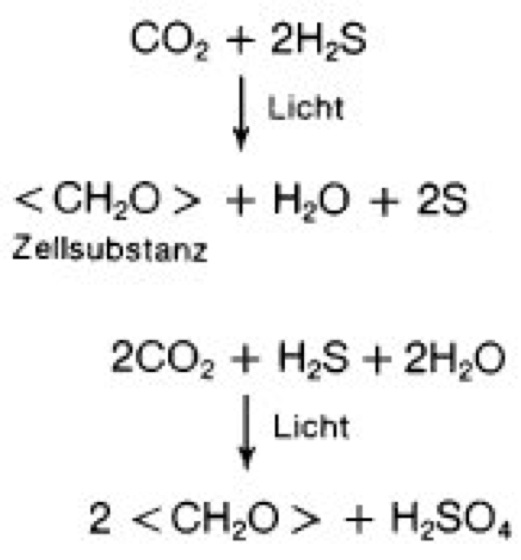
phototrophe Bakterien
Abb. 3: Photosynthesegleichungen des Schwefelpurpurbakteriums Chromatium

phototrophe Bakterien
Abb. 4:Photosyntheseapparat, Aufbau eines lichtgetriebenen Protonengradienten und ATP-Bildung bei anoxygenen Purpurbakterien.
Der Photosyntheseapparat der Purpurbakterien enthält membrangebundene Pigment-Proteinkomplexe (Carotinoide, Bakteriochlorophylle [BChl]), Redoxkomponenten als Elektronen- bzw. Wasserstoffüberträger und den ATP-Synthase-Komplex (mitochondrialer Kopplungsfaktor). Der größte Teil der photosynthetischen Pigmente, die Antennenpigmente (Carotinoide, B-Bakteriochlorophyll), liegt in den Antennenkomplexen I und II (= LHC I, LHC II [Light Harvesting Complex]. Antennenkomplex I (B870, LHC I) umgibt das photochemische Reaktionszentrum, zusätzlich wird bei den meisten Purpurbakterien noch ein variabler Antennenkomplex II (B800–850, LHC II) gebildet, dessen Ausprägung besonders von der Lichtintensität abhängt. Das photosynthetische Reaktionszentrum (RZ) enthält ein Dimer des Reaktionszentrum-Bakteriochlorophylls (a oder b), ([BChl]2, P870), das auch als „besonderes Paar“ (engl. „special pair“) bezeichnet wird, dazu Proteinuntereinheiten, akzessorisches BChl, Bakteriophäophytin [Bphe], Chinone [Q] (meist Ubichinon) und ein Eisenatom. – Die von den Antennenpigmenten absorbierte Lichtenergie wird als Anregungsenergie (Excitonen-Übertrag) an das Reaktionszentrum-(BChl)2-P870 weitergeleitet; dadurch wird P870 in einen angeregten Zustand P870* überführt und somit in einen starken Elektronendonor umgewandelt. Vor der Anregung beträgt das Redoxpotential (E0´) von P870 +0,5 V, nach der Anregung etwa –1,0 V, d.h., es weist einen sehr großen Gehalt an freier Energie auf. P870* setzt 1 Elektron von hohem (negativem) Reduktionspotential frei, das an eine Serie von Elektronenüberträgern weitergegeben wird. Redoxkomponenten im Reaktionszentrum sind BChl, Bphe und 2 Chinone (an der cytoplasmatischen Seite der Membran). Durch die weitere Aufnahme eines Elektrons vom angeregten P870* und die Aufnahme von 2H+ von der cytoplasmatischen Seite der Membran wird Chinon reduziert (QH2). Es erfolgt dann ein Austausch mit dem Chinonpool. Anschließend fallen die Elektronen über eine Reihe von Eisen-Schwefel-Proteinen und Cytochrome auf das P870 zurück. Wichtige Elektronentransportkomponenten sind dabei der Cytochrom-bc1-Komplex und das periplasmatische Cytochrom c2, das zum Auffüllen des Elektronenlochs im aktiven Zentrum dient. Da bei diesem Elektronenfluß keine Nettozufuhr und kein Verbrauch an Elektronen stattfindet, liegt ein zyklischer Elektronentransport vor, der durch das Licht kontinuierlich angetrieben wird. Während des Abfalls der Elektronen vom P870* auf die Stufe des Cytochroms c2, über Elektronen- und Wasserstoffüberträger, werden Protonen aus dem Cytoplasma in die Kette aufgenommen und in den Innenraum (Periplasma) der Vesikel abgegeben, so daß ein Protonengradient über der Thylakoidmembran entsteht (ähnlich wie bei der Atmungskette). Der Protonengradient dient direkt als Energiequelle (z.B. für Geißelbewegung, einige Substrataufnahmen) oder wird zur ATP-Bildung über die ATP-Synthase (ATPase-System) genutzt. Dieser ATP-Gewinn wird als zyklische Photophosphorylierung bezeichnet, da er an den zyklisch verlaufenden Elektronentransport (Photosystem II) gekoppelt ist (Gegensatz Photosynthese der Cyanobakterien und grünen Pflanzen). – Die Bildung von Reduktionsäquivalenten [NAD(P)H] zur Reduktion von Kohlendioxid oder anderen oxidierten Kohlenstoffquellen kann aus energetischen Gründen bei den Purpurbakterien nicht durch eine Lichtreaktion erfolgen (absorbiertes Licht zu langwellig). Bei diesen phototrophen Bakterien wird NAD(P)H daher anaerob durch einen rückläufigen Elektronentransport über Komponenten der Atmungskette gebildet (wie bei nitrifizierenden Bakterien). Licht liefert bei dieser Reduktion nur die notwendige Energie (ATP). Externe Elektronendonoren für die Kohlenstoffassimilation sind reduzierte Schwefelverbindungen, Fe2+, H2 und zum Teil auch organische Substrate, deren Elektronen über Cytochrom c2 eingeschleust werden. – Die grünen Bakterien und Heliobakterien (z.B. Gattung Heliobacterium), die Licht kürzerer Wellenlänge absorbieren, können dagegen NAD(P)+ direkt im Lichtstoffwechsel reduzieren (nichtzyklischer Elektronentransport).
AI, AII = Antennenkomplex I und II (Bakteriochlorophyll a, Carotinoide), B800, B850, B870 = Antennen-Bakteriochloropylle, BC1 = Cytochrom-bc1-Komplex, bc1 = Cytochrome b und c1, BChl = Bakteriochlorophyll, Bphe = Bakteriophäophytin, c2 = Cytochrom c2, e– = Elektron, Fe-S = Schwefel-Eisen-Protein, P870 = Reaktionszentrum-Bakteriochlorophyll-a-Dimer, P870* = von Licht angeregtes P870, Pi = anorganisches Phosphat, Q = Ubichinon oder Menachinon, QH2 = reduziertes Chinon, RZ-Komplex = Reaktionszentrum-Komplex.
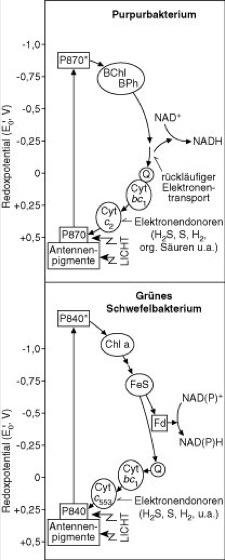
phototrophe Bakterien
Abb. 5: Schema des Elektronenflusses bei Purpurbakterien und grünen Schwefelbakterien.
Beide Gruppen phototropher Bakterien führen nach der Anregung durch Licht einen zyklischen Elektronenfluß vom dimeren Reaktionszentrum-Bakteriochlorophyll P870 bzw. P840 über verschiedene Elektronen und Wasserstoffüberträger durch. Dabei wird ein Protonengradient über die Thylakoidmembran bzw. Cytoplasmamembran ausgebildet, durch den eine ATP-Synthese stattfindet. – Die Bildung von Reduktionsäquivalenten [NAD(P)H] zur Reduktion von Kohlendioxid im phototrophen Stoffwechsel verläuft dagegen unterschiedlich. Während bei den Purpurbakterien ein rückläufiger Elektronentransport notwendig ist, der durch den Protonengradienten bzw. ATP aus den Lichtreaktionen entsteht, kann bei den grünen Schwefelbakterien NAD(P)H auch in einer direkten Lichtreaktion gebildet werden; dabei sind auch Chlorophyll a (Chl a), eventuell ein Chinon, ferner ein Schwefel-Eisen-Protein (FeS) und Ferredoxin (Fd) als Elektronenüberträger mitbeteiligt. Bei der NAD(P)H-Bildung findet somit ein nichtzyklischer, also offenkettiger Elektronentransport statt, an dem aber kein ATP gebildet wird. Elektronendonoren zur Reduktion von NAD(P)+ sind reduzierte Schwefelverbindungen oder Wasserstoff.
Antennenpigmente = Bakteriochlorophylle und Carotinoide, BChl = Bakteriochlorophyll, Chl a = Chlorophyll-a-Isomer, Cyt bc1 = Cytochrom b und c1, Cyt c2 = periplasmatisches Cytochrom c2, Fd = Ferredoxin, Fe-S = Schwefel-Eisen-Protein, P870, P840 = Reaktionszentrum-Bakteriochlorophyll-Dimer, P870*, P840* = durch Licht angeregtes P870 und P840, Q = Chinone (Ubichinon).
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.