Lexikon der Neurowissenschaft: Drosophila-Nervensystem
Drosophila-Nervensystem, E Drosophila nervous system, das Nervensystem der in der Biologie als Modellorganismus verwendeten kleinen Taufliege Drosophila melanogaster, ein typisches Insekten-Nervensystem. Das Zentralnervensystem (Übersicht siehe Abb. 1 ) besteht aus einem Gehirn ( siehe Abb. 2 ; siehe Abb. 3 ), das in ein Oberschlundganglion und ein Unterschlundganglion unterteilt wird, aus einem ventralen Nervenstrang, der aus segmentalen Ganglien besteht, und aus einem stomatogastrischen Nervensystem. Die sensorischen Sensillen, die man in externe Sinnesorgane, Chordotonalorgane und multidendritische Neurone unterteilt, sowie die Axone der Motoneurone und neuroendokrinen Zellen stellen zusammengenommen das periphere Nervensystem dar. Die optischen Loben (Lobus opticus), in Lamina, Medulla und Lobula/Lobulaplatte unterteilt, sind mit dem rostralen Teil des Gehirns assoziiert und beinhalten mehr Nervenzellen als das ganze übrige Nervensystem; sie erhalten ihren Eingang von den großen, hochdifferenzierten Komplexaugen, die meist ebenfalls dem peripheren Nervensystem zugeteilt werden ( siehe Abb. 4 ). Die besondere Bedeutung des Nervensystems von Drosophila für die neurowissenschaftliche Forschung liegt darin, daß es als leistungsfähiges Modellsystem für neurogenetische Untersuchungen Verwendung findet. – Die Entwicklung des Nervensystems ist bei Drosophila besonders gut untersucht. Dabei hat sich gezeigt, daß die molekulargenetische Kontrolle der neuronalen Entwicklung bei Drosophila und bei höheren Vertebraten erstaunlich ähnlich abläuft. Im ersten Schritt der Drosophila-Neurogenese erhalten selektive Bezirke des embryonalen Ektoderms durch die Expression von proneuralen Genen die Kompetenz, sich zu Neuronen zu entwickeln. In einem zweiten Schritt entstehen aus diesem Neuroektoderm unter der Einwirkung der neurogenen Gene die einzelnen Stammzellen der Neurone und der Glia. Schließlich bestimmen neuronenspezifische Gene die Differenzierung dieser Zellen. Die allermeisten Nervenzellen im Zentralnervensystem entstehen in stereotyper Weise durch asymmetrische Zellteilungen aus diesen großen Stammzellen, die Neuroblasten genannt werden. Dabei entsteht bei jeder Zellteilung eines Neuroblasten eine Ganglienmutterzelle, die sich einmal symmetrisch teilt und dabei zwei postmitotische Nervenzellen hervorbringt. Etwa 800 Neuroblasten erzeugen die Nervenzellen der Segmentalganglienkette, etwa 150 Neuroblasten erzeugen die Nervenzellen des Gehirns. Bei der Embryonalentwicklung entstehen identifizierbare Nervenzellen in jedem Segmentalganglion durch die proliferative Aktivität von etwa 50 Neuroblasten, die als zelluläre Individuen angesprochen werden können und deren Identität auf jeweils charakteristische Kombinationen von regulatorischer Genexpression zurückgeführt werden kann. Während der nachfolgenden Larvalentwicklung wird die proliferative Aktivität der Neuroblasten fortgesetzt, und es kommt zur Bildung von vielen weiteren, noch weitgehend undifferenzierten Nervenzellen (besonders in den optischen Loben) sowie zu einer Fusionierung von Gehirn und Segmentalganglien ( siehe Abb. 5 ). Bei der anschließenden Metamorphose kommt es zu drastischen Umwandlungen im Nervensystem sowie zur Ausdifferenzierung von einer Vielzahl von Nervenzellen mit dem Ergebnis, daß das adulte Nervensystem 10-20fach mehr funktionsfähige Nervenzellen aufweist als das larvale Nervensystem. Es kommt zu einer markanten Vergrößerung des Gehirns und besonders der optischen Loben, der Antennalloben und der Pilzkörper. Im ventralen Nervenstrang findet eine Regression der abdominalen Ganglien und eine Expansion der thorakalen Ganglien statt. Die sensorischen Sensillen des peripheren Nervensystems entstehen weitgehend neu. – Zusätzlich zur Neurogenese, die zur Bildung von Nervenzellen führt, müssen bei der Entwicklung des Zentralnervensystems Regionalisierungsprozesse ablaufen. Diese sind einmal durch die Segmentierungsvorgänge gegeben, die nicht nur die Körpersegmentierung von Drosophila hervorbringen, sondern auch zur Bildung der metameren Ganglien des ventralen Nervensystems führen. Bei der Gehirnentwicklung treten darüber hinaus weitere Regionalisierungsvorgänge auf, die durch zahlreiche Kontrollgene, deren Produkte selektiv in der Kopfregion exprimiert werden, gesteuert werden. Hierzu gehören zwei Homöobox-Gene, orthodenticle und empty-spiracles, die als anteriore gap-Gene und homöotische Selektorgene für den vorderen Kopfbereich wirken. Diese beiden Gene steuern im Oberschlundganglion unter anderem die Expression der proneuralen Gene, welche wiederum die neurogenen Gene aktivieren. Im Unterschlundganglion wird die regionalisierte Identität durch die Einwirkung der homöotischen Gene kontrolliert. Bemerkenswerterweise sind die Expressionsdomänen der orthologen (entsprechenden) gap-Gene und homöotischen Gene in den Gehirnanlagen von Drosophila und Maus sehr ähnlich. Diese Tatsache sowie der Befund, daß Mutationen in orthologen Genen zu ähnlichen Gehirnphänotypen in Drosophila und Maus führen, gibt Anlaß zur Hypothese der monophyletischen Entstehung der Gehirne von Arthropoden und Wirbeltieren. – Die Entwicklung der Komplexaugen bei Drosophila hat in den letzten Jahren besonderen Modellcharakter erlangt. Ein adultes Komplexauge besteht aus etwa 800 regelmäßig angeordneten Ommatidien ( siehe Abb. 6 ). Jedes Ommatidium besteht aus 20 Zellen, wobei acht davon die photorezipierenden Retinulazellen sind. Wie die meisten externen Organe der adulten Drosophila, entwickeln sich die Komplexaugen aus Primordien, den sogenannten Imaginalscheiben. Während der Augenentwicklung proliferiert das zunächst noch undifferenzierte Epithel der entsprechenden Imaginalscheibe. Im späteren Larvenstadium beginnt dann ein morphogenetisches Differenzierungsprogramm, bei dem in räumlich und zeitlich festgelegter Abfolge im Augenprimordium alle Ommatidien in der korrekten Musteranlage entstehen, wobei die Differenzierung der einzelnen Zelltypen in jedem Ommatidium sukzessive nach festgelegter Reihenfolge erfolgt. Bei der Differenzierung der Zellen in einem Ommatidium spielen Zell-Zell-Wechselwirkungen und intrazelluläre Signaltransduktionsprozesse (Singaltransduktion) eine entscheidende Rolle. Es ist bemerkenswert, daß der gesamte morphogenetische Ablauf, der zur Augenbildung führt, durch ektopische Expression von bestimmten Regulatorgenen wie das eyeless/Pax6 Gen ausgelöst werden kann, sogar an Antennen oder Beinen. – Nach erfolgter Neurogenese müssen die erzeugten Nervenzellen Axone ausbilden (Axogenese), die beim Auswachsen selektive Wegfindung und Zielerkennung durchführen müssen (axon guidance). Die genetische Analyse dieses Vorgangs bei Drosophila zeigt, daß eine Vielfalt von molekularen Mechanismen beteiligt ist. Die Bedeutung von Substratadhäsionsmolekülen wie Tenascin, von Zelladhäsionsmolekülen wie den Cadherinen oder bestimmten Mitgliedern der Immunglobulingen-Superfamilie, sowie von Zell-gebundenen diffusiblen Attraktantien und Repellentien wie den Netrinen sind bei Drosophila durch elegante Mutantenanalysen untersucht worden. Durch Mehrfachmutanten konnte gezeigt werden, daß redundante Absicherungen des axonalen Wegfindungsprozesses vorliegen. Wie bei der Neurogenese wird auch bei der molekularen Analyse der Axogenese klar, daß die genetische Kontrolle der neuronalen Entwicklung bei Drosophila und bei höheren Vertebraten sehr ähnlich abläuft. – Neben der genetischen Analyse der neuronalen Entwicklung gibt es eine Reihe von neurogenetischen Untersuchungen, die am adulten Nervensystem bzw. bei der Verhaltensanalyse (Verhalten) an Drosophila durchgeführt wurden. So sind durch Mutantenanalysen viele der Gene, die bei der Steuerung des Sexualverhaltens bei Drosophila beteiligt sind, entdeckt worden. Einige dieser Gene werden geschlechtsspezifisch in den Pilzkörpern des Gehirns exprimiert. Die Pilzkörper sind prominente integrative Strukturen im Fliegengehirn, die sowohl der Verarbeitung von olfaktorischer Information dienen, als auch offenbar der Sitz für zahlreiche Aspekte des Sexualverhaltens sind ( siehe Abb. 7 ). Bei der genetischen Analyse der biologischen Rhythmik haben Mosaikanalysen bei Drosophila nachgewiesen, daß spezifische Gehirnareale als Sitz der circadianen Oszillatoren funktionieren. Eine vertiefte Mutantenanalyse der circadianen Periodik (circadianer Rhythmus) in der Fliege hat zur molekularen Aufklärung der wichtigsten zeitgebenden Oszillatoren und der daran beteiligten Gene period und timeless geführt. – Die genetische Analyse von Lernmechanismen (Lernen) in Drosophila, insbesonders die Entdeckung und Charakterisierung von zahlreichen Lernmutanten, hat Einsichten in die molekularen Grundlagen sowohl von einfachen Lernformen wie Habituation und Sensitivierung als auch von komplexeren Lernformen wie klassische und operante Konditionierung ergeben. Zum Beispiel konnte gezeigt werden, daß zwei gut untersuchte Lernmutanten, dunce und rutabaga, welche Defizite in einfachem Lernverhalten aufweisen, spezifische Defekte im cAMP-Stoffwechsel haben. dunce codiert für eine Phosphodiesterase, die cAMP in 5'-AMP spaltet, und rutabaga ist das Strukturgen für eine Ca2+/Calmodulin-abhängige Adenylatcyclase, die cAMP aus ATP herstellt. Dies unterstützt Studien, die bereits die Beteiligung des cAMP-Stoffwechsels an Lernvorgängen in der Meeresschnecke Aplysia nahegelegt hatten. Mutantenanalysen haben auch Gehirnareale identifiziert, die für Lernen essentiell sind. Beispielsweise konnte die zentrale Beteiligung des Pilzkörpers an Lernprozessen, die auf der Konditionierbarkeit auf olfaktorische Reize beruhen, durch Studien an Mutanten nachgewiesen werden. Schließlich haben neurogenetische Studien an Drosophila zur Entdeckung von molekularen Veränderungen geführt, die bei der synaptischen Plastizität während einfacher Lernvorgänge ablaufen. So konnte gezeigt werden, daß sich synaptische Plastizität in eine strukturelle und eine funktionelle Komponente unterteilen läßt, daß diese Komponenten genetisch separierbar sind, und daß beide zur Verstärkung von Synapsen erforderlich sind. Dabei beruht die strukturelle Komponente auf Änderungen in der Menge von Zelladhäsionsmolekülen, während die funktionelle Komponente auf einer CREB-initiierten Genkaskade beruht. Plastizität im Nervensystem.
Lit.:Campos-Ortega, J.A.,Hartenstein, V.: The Embryonic Development of Drosophila Melanogaster. Berlin, 1997. Greenspan, R.J.: Understanding the Genetic Construction of Behaviour. Scientific American 272:74-79 (1995). Goodman, C.S.: Mechanisms and Molecules that Control Growth Cone Guidance. Annual Review of Neuroscience 19:341-377 (1996).
Eine umfangreiche Sammlung von Darstellungen des Nervensystems von Drosophila ist "flybrain online" (http://www.flybrain.org).
H.R./K.F.F.

Drosophila-Nervensystem
Abb. 1: Horizontaler Schnitt durch das gesamte ZNS einer Fliege: Darstellung der Riesenfasern in der Enhancer Trap-Linie 307
In diesem Schnitt durch das ZNS einer transformanten Drosophila sind nur sehr wenige Zellkörper (anterior dorsal cell body, ADCB, und giant fiber cell body, GFCB) durch die Expression eines Reportergens (lacZ) markiert. GFCB ist der Zellkörper der sogenannten Riesenfaser, die ihr Axon durch das Halskonnektiv (Konn) in das Bauchmark sendet. Dieses wird durch die Verschmelzung der thorakalen Ganglien in den drei Thorakalsegmenten T1, T2, T3 und der abdominalen Ganglien (Abd) gebildet (mit freundlicher Genehmigung von Dr. K.G. Moffat, Warwick, aus: www.flybrain.org, accession no. AA00098).

Drosophila-Nervensystem
Abb. 2: Posteriore Ansicht eines Ganz-Gehirn-Präparats einer Drosophila (dorsal ist oben)
Ein Antikörper gegen Synaptotagmin, ein synaptisches Protein, wurde verwendet, um synaptisches Neuropil im Konfokalmikroskop sichtbar zu machen. Lateral sind (als einzige nicht synaptische Strukturen) die Corneae der Ommatidien des Komplexauges markiert. Darunter schließt sich der optische Lobus an, der aus Lamina (la), der äußeren Medulla (me o), der inneren Medulla (me i), der Lobula (lo) und der Lobulaplatte (lo p) besteht. Das Zentralhirn, hervorgegangen aus der Verschmelzung von Ober- und Unterschlundganglion (su oes g), wird von dem Oesophagus durchzogen (oes). Gut sichtbar ist die Pars intercerebralis (pars in), eine zentrale Zellkörperregion, der Calyx der Pilzkörper (ca), die protocerebrale Brücke (pr br), das laterale Horn (l ho) und das posteriore, laterale Deutocerebrum (p l deu). (mit freundlicher Genehmigung von Dr. Xuejun Sun, Halifax, aus: www.flybrain.org, accession no. AC00158)
Drosophila-Nervensystem
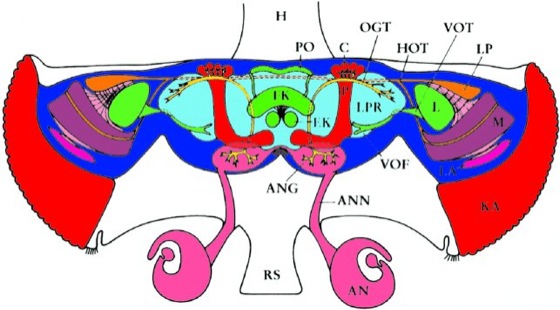
Abb. 3: Gehirnschema
Schematische Aufsicht auf das Gehirn einer Drosophila. Zwischen den Komplexaugen (KA) liegt das bilateral symmetrische Fliegengehirn. Die peripher gelegenen Zellkörper (dunkelblau) sind deutlich von den Neuropilregionen, die die Axone und Dendriten beherbergen, abgesetzt. Direkt unterhalb eines Komplexauges liegt der optische Lobus, der sich in die Neuropilbereiche Lamina (LA), Medulla (M), Lobula (L) und Lobulaplatte (LP) untergliedert. Der vordere optische Trakt (VOT) verbindet die Lobula mit dem vorderen optischen Fokus (VOF) im lateralen Protocerebrum (LPR). Der hintere optische Trakt (HOT) enthält Fasern, die z.T. bis in den contralateralen optischen Lobus verlaufen. Die Pilzkörper (hellrot) sind wichtige Strukturen des Zentralhirns, die von den Kenyonzellen gebildet werden. Diese erhalten ihren Input über den Tractus olfactorius (OGT) aus dem Antennenganglion (ANG) in der Calyxregion (C) und senden ihre Axone durch den Pedunkel (P) ins vordere Gehirn. Der Zentralkomplex (grün) im Gehirnzentrum besteht aus der Brücke (Pons, PO), dem fächerförmigen Körper (FK) und dem Ellipsoidkörper (EK). Der Antennennerv (ANN) enthält sowohl die Axone olfaktorischer als auch mechanosensorischer Sinneszellen auf den Antennen (AN). RS, Rüssel; H, Hals.

Drosophila-Nervensystem
Abb. 4: Horizontaler Semidünnschnitt durch den optischen Lobus
Semidünnschnitt (1,5 μm) durch den optischen Lobus von Drosophila. Die Untergliederung in Lamina (La), Medulla (Me), Lobula (Lo) und Lobulaplatte (LP) ist sehr gut sichtbar, ebenso wie die Tatsache, daß die Zellkörper der Nervenzellen in der Peripherie positioniert sind, während ihre Fortsätze das dichte Neuropil ausbilden. Die "Tintenkleckse" sind eine Subpopulation von Gliazellen, die das bakterielle Enzym β-Galactosidase exprimieren. In den optischen Chiasmata sind besonders große Gliazellen auszumachen, kleinere säumen z.B. die distale Oberfläche der Medulla.

Drosophila-Nervensystem
Abb. 5: Scanning-elektronenmikroskopisches Bild des ZNS einer Drosophilalarva kurz vor der Verpuppung
Von der ursprünglichen strickleiterartigen Anlage des Insekten-ZNS ist bei der Drosophilalarve bei oberflächlicher Betrachtung nicht viel zu sehen. In diesem elektronenmikroskopischen Präparat des gesamten ZNS einer Larva im dritten Häutungsstadium ist die kugelige Form der Gehirnhemisphären (GH) gut sichtbar. Auch der ventral gelegene Zapfen (Z), hervorgegangen aus dem Verschmelzen der Thorakal- und Abdominalganglien, ist an der Oberfläche kaum gegliedert. Seine darunterliegende segmentale Organisation wird jedoch z.B. durch die Lage der Beinnerven (BN) deutlich. Die Augenimaginalscheiben (AA), aus der die Komplexaugen der Fliege entstehen werden, liegen anterior zu den Hemisphären. Der optische Stiel (OS), durch den die Retinulazellaxone begonnen haben, in das Gehirn einzuwachsen, verbindet eine Augenimaginalscheibe mit der dazugehörigen Hemisphäre. Mit freundlicher Genehmigung von Prof. Dr. G. Technau (Mainz).

Drosophila-Nervensystem
Abb. 6: Querschnitt durch das Komplexauge
Dieser Querschnitt durch das Komplexauge von Drosophila zeigt dessen quasi kristalline, repetitive Struktur. Ein Komplexauge besteht bei Drosophila aus etwa 800 Ommatidien, den Facetten. Innerhalb der Ommatidien ist die regelmäßige Anordnung der 7 Rhabdomere, der lichtleitenden und das Sehpigment enthaltenden Strukturen, erkennbar. Jede Zelle eines Ommatidiums hat ihren festen Platz. Hierdurch wird die präzise Ausrichtung der optischen Achsen der 7 Rhabdomere des Fliegenommatidiums sichergestellt. Die sechs äußeren Rhabdomerquerschnitte mit etwas größerem Radius werden von den Retinulazellen R1-6 gebildet, das innere, dünnere Rhabdomer wird distal von der Zelle R7 und proximal von der Zelle R8 produziert.
Drosophila-Nervensystem
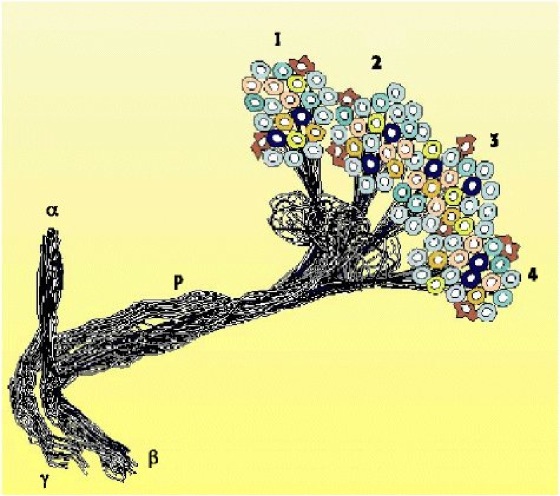
Abb. 7: Pilzkörper
Schematischer Aufbau eines Pilzkörpers, einer auffälligen Struktur in jeder Hälfte des Fliegengehirns, deren Beteiligung an Lernprozessen nachgewiesen ist. Gebildet wird der Pilzkörper von etwa 1000 Kenyonzellen, den Nachkommen von 4 Neuroblasten. Obwohl verschiedene Typen von Kenyonzellen existieren (wie durch die unterschiedliche Farbgebung der Zellkörper verdeutlicht werden soll), sind die Zellklone (1-4) äquivalent. Gemeinsame Merkmale der Kenyonzellen sind die Position ihrer Zellkörper (hinten oben im Gehirn), die Ausbildung dendritischer Spezialisierungen im sogenannten Calyx-(Hut-) Bereich, der viele prominente axonale Terminalien von olfaktorischen Interneuronen enthält, sowie ein langes Axon, welches durch den Pedunkel (P) von hinten oben quer durch das Gehirn nach vorne unten zieht. Die Axone bilden dort in den alpha-(α), beta-(β) und gamma-(γ) Loben ihre Terminalien aus (mit freundlicher Genehmigung von Dr. Kei Ito aus: www.flybrain.org, accession no. AB00151).
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.