Selbstorganisation: Künstliche Proteinkapseln setzen sich selbst zusammen
Molekulare Maschinen kann man nicht einfach zusammenbauen – für die Mechanik sind sie zu klein und für chemische Verfahren schon viel zu komplex. Damit aus submikroskopisch winzigen Einzelteilen Strukturen wie nanostrukturierte Materialien, Mikrokapseln oder gar komplexe mechanische Maschinen wie die Bakteriengeißel werden, müssen sich die Einzelteile schon selbsttätig zusammenfügen.
Lebende Zellen zeigen, dass diese selbstorganisierten Strukturen prinzipiell beliebig kompliziert werden können. Allerdings ist die Technik hier noch lange nicht so weit wie die Biologie. Forscher müssen bisher auf eher rabiate Methoden zurückgreifen, um die Einzelmoleküle zusammenzuzwingen – zum Beispiel über komplexierte Metallatome, reaktive Molekülgruppen oder gar von anderen Proteinen zweckentfremdete Eiweißstrukturen. Lediglich bei der DNA sind derzeit gerichtete Verbindungen mit natürlichen Methoden erreichbar: Als Kontaktstellen produziert man einfach Einzelstränge mit komplementären Sequenzen.
Natürliche Proteininteraktionen, wie sie in den Proteinclustern der Zelle vorkommen, basieren dagegen auf einer Vielzahl schwacher, aber komplexer Effekte, die nur sehr schwer vorauszuberechnen sind. Damit sich Proteine durch diese Wechselwirkung selbst organisieren, müssen die Bindungskräfte nicht nur stark genug sein, um die Proteine aneinander zu binden, sondern auch stärker als alle denkbaren anderen Kontakte, die sich durch Zufall ergeben könnten. Dazu müssen die Oberflächen beider Partner präzise zusammenpassen – und diese Präzision auf der Ebene einzelner Atome konnten Molekülmodelle bisher nicht liefern. Erst jetzt ist es Forschern aus den USA mit modernsten Computertechnologien gelungen, auch künstlich veränderte Eiweißmoleküle nach dem Vorbild der Natur zu vorherbestimmten Formen zu sortieren.
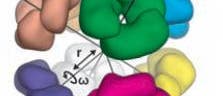
Das Team um David Baker von der University of Washington in Seattle konzentrierte sich auf hochgradig symmetrische Hohlkapseln mit einer dreifachen Symmetrieachse und verwendete als Ausgangspunkt Proteine, die sich von Natur aus zu Trimeren zusammenlagern. So mussten sie am Protein selbst nur einen Bereich modifizieren, um die Selbstorganisation von 24 der Einzelproteine zur Kapselstruktur zu steuern.
Die Forscher arrangierten im Computer die Trimere von 271 Proteinen in der gewünschten Kapselstruktur und sortierten jene aus, bei denen sich die Peptidgerüste überschnitten. Für die verbleibenden Kandidaten berechneten die Forscher dann veränderte Aminosäuresequenzen mit stärkeren Interaktionen an der Kontaktstelle und optimierten sie weiter, unter anderem mit Hilfe des Computerspiels FoldIt. Schließlich blieben 33 Proteinvarianten auf der Basis von 15 Proteinen übrig, die das Forscherteam in Bakterien herstellte. Dann überprüften sie, ob diese hielten, was das Computermodell versprach.
Tatsächlich erwies sich eines der Proteine als tauglich: Im Experiment vereinten sich 24 Untereinheiten selbsttätig zu einer Oktaederstruktur, die sehr genau der Vorhersage im Computer entsprach. Das gleiche gelang den Forschern auch mit einer kleineren, tetraedrischen Struktur aus 12 Untereinheiten. Die Forscher betonen, dass sich das Designprinzip neben Kapseln auch auf zwei- oder dreidimensional ausgedehnte Strukturen anwenden lässt. Allerdings sollten diese ebenfalls sehr symmetrisch sein, denn mit abnehmender Symmetrie steigt der Aufwand beim Konstruieren der miteinander wechselwirkenden Bereiche stark an.

Schreiben Sie uns!
Beitrag schreiben