Lexikon der Ernährung: Gluconeogenese
Gluconeogenese, E gluconeogenesis, die Biosynthese von Glucose aus Nicht-Kohlehydratvorstufen in Leber und Niere. Zusammen mit der Zufuhr von Glucose – exogen durch die Nahrung, endogen durch die Glycogenolyse – stellt die G. den dritten wichtigen Faktor zur Homöostase der Glucosekonzentration im Blut dar (Blutzuckerregulation). Sie ist außerdem bei starkem Lactatanfall durch Muskelarbeit (Cori-Zyklus) von Bedeutung. Als Substrate der G. dienen Lactat aus Muskulatur und Erythrocyten, Glycerin (vgl. α-Glycerophosphat, Glycerophosphat-Dehydrogenase, Triosen) aus dem Fettgewebe sowie die glucogenen Aminosäuren (= glucoplastische Aminosäuren: Alanin, Serin, Glycin, Threonin, Cystein, Asparaginsäure, Glutaminsäure, Arginin, Histidin, Prolin, Valin).
Prinzipiell werden die Reaktionen der Glycolyse bei der G., die ebenfalls im Cytosol lokalisiert ist, in umgekehrter Richtung durchlaufen (Abb.). Da die ATP-verbrauchenden Reaktionen aus energetischen Gründen nicht umkehrbar sind, werden diese drei Schritte von spezifischen Enzymen der G. katalysiert.
1) Pyruvat wird in zwei Reaktionen durch die Katalyse der mitochondrialen Pyruvatcarboxylase und der cytosolischen Phosphoenolpyruvat-Carboxykinase in Phosphoenolpyruvat umgewandelt.
2) Fructose-1,6-diphosphatase katalysiert die Bildung von Fructose-6-phosphat aus Fructose-1,6-diphosphat. Das Enzym wird durch Fructose-2,6-diphosphat (zugleich Aktivator des Glycolyse-Enzyms Phosphofructokinase) gehemmt, dessen Konzentration unter der Kontrolle von Glucagon steht.
3) Fructose-6-phosphat steht im Gleichgewicht mit Glucose-6-phosphat und dieses kann zum einen über Glucose-1-phosphat der Glycogensynthese dienen, oder zum anderen durch Glucose-6-phosphatase in Phosphat und Glucose gespalten werden. Da dieses Enzym nur in Leber, Niere und (geringe Aktivität) in der Mucosa des Darmes vorkommt, können nur diese Gewebe – vor allem die Leber – Glucose für andere Organe bereitstellen.
Die Regulation von G. und Glycolyse greift an den Schlüsselreaktionen an, in denen sie sich unterscheiden. Schlüsselenzym für die G. ist in erster Linie die Phosphoenolpyruvat-Carboxykinase. Alle Schlüsselenzyme der G. werden durch Insulin gehemmt und durch Glucagon, Glucocorticoide und Catecholamine induziert. Ausgehend von Pyruvat werden 6 Mol ATP pro Mol Glucose verbraucht. Die Anbindung an den Fructose-Stoffwechsel erfolgt auf der Stufe des Dihydroxyacetonphosphats. Orale Antidiabetika wie z. B. Biguanide wirken z. T. über eine Hemmung der G. Der im Rahmen des Alkoholstoffwechsels erhöhte NADH + H+ / NAD+-Quotient bewirkt, dass Pyruvat vermehrt in Lactat umgewandelt wird und drosselt so die G. Da Alkohol auch in sog. Diabetiker-Bier und Diabetiker-Wein enthalten ist, kann es nach Genuss dieser Getränke zu einer Hypoglycämie kommen.
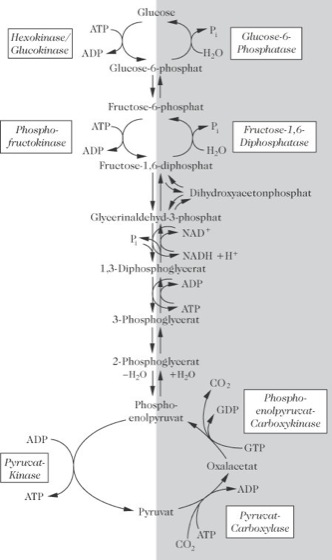
Gluconeogenese: Reaktionen und Schlüsselenzyme der Glycolyse (links) und Gluconeogenese (rechts) im Vergleich. [n. G. Rehner u. H. Daniel, Biochemie der Ernährung, Spektrum Akademischer Verlag, Heidelberg, 1999] Gluconeogenese
Schreiben Sie uns!