Lexikon der Biologie: Lymphocyten
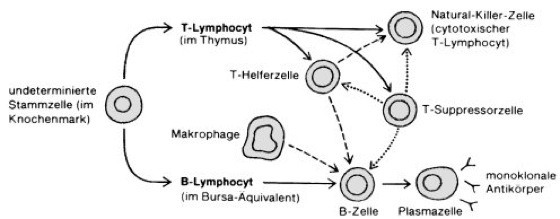
Lymphocyten [von *lympho- , griech. kytos = Höhlung, Zelle], Lymphzellen, Gruppe der Leukocyten (Immunzellen, Immunsystem), ca. 7–9 μm große weiße Blutkörperchen, die im mikroskopischen Bild mit einem schmalen Plasmasaum um den runden Kern erkennbar sind (Blutzellen). Lymphocyten ( vgl. Abb. 1 ) machen ca. 20–55% der Leukocyten aus und sind die Mediatoren der adaptiven Immunität. Die Gesamtzahl der Lymphocyten eines erwachsenen Menschen beträgt ca. 1 ·1012, wobei pro Tag ca. 109 Lymphocyten produziert werden. Die lymphoiden Stammzellen im Knochenmark können sich zu B-Lymphocyten (B-Zellen) und T-Lymphocyten (T-Zellen) entwickeln ( vgl. Abb. 2 ), wobei die B-Zell-Entwicklung im Knochenmark stattfindet, T-Zell-Vorläufer jedoch in einem frühen Stadium in den Thymus auswandern (lymphatische Organe), wo sie zu T-Lymphocyten differenzieren. B-Zellen (benannt nach der Bursa Fabricii, Bursa-Äquivalent) sind antikörperproduzierende Zellen (Antikörper, monoklonale Antikörper, Milz), welche für die humorale Immunabwehr (humorale Immunität) von entscheidender Bedeutung sind. Nach Kontakt mit einem Antigen differenzieren sie nach Interaktion mit Makrophagen zu sog. Plasmazellen und produzieren typische, speziell gegen das jeweilige Antigen gerichtete Antikörper (Immunglobuline). Diese Zellen stellen spezialisierte Klone dar, die jeweils nur auf ein bestimmtes Antigen reagieren. Reife B-Zellen können des weiteren in B-1-B-Zellen und B-2-B-Zellen oder „konventionelle" Zellen unterteilt werden. B-1-B-Zellen zeichnen sich durch die Expression des Oberflächenmarkers CD5 (CD-Marker) und durch niedrig-affine polyspezifische B-Zell-Rezeptoren aus. Sie kommen gehäuft in den peritonealen und pleuralen Kavitäten (Hohlräumen) vor und sind von klinischem Interesse, da sie die Ausgangszellen der chronisch-lymphatischen Leukämie (CLL) sind. T-Zellen stellen die zellulären Abwehrmechanismen der adaptiven Immunantwort und können weiter in γ-δ-T-Zellen und α-β-T-Zellen unterteilt werden. Hierbei entsprechen α-β-T-Zellen den „konventionellen" T-Zellen, während die Erkenntnisse über γ-δ-T-Zellen noch begrenzt sind. γ-δ-T-Zellen entwickeln sich, wie auch B-1-B-Zellen, früh in der Ontogenese und sind anatomisch auf die Epidermis, Epithelien und den Urogenitaltrakt (Urogenitalsystem) beschränkt. Die sehr gut untersuchten α-β-T-Zellen können in sog. T-Helfer-Zellen (CD4+; Helfer-Zellen) und cytotoxische T-Lymphocyten (CD8+) unterteilt werden. Cytotoxische T-Zellen können mittels ihres T-Zell-Rezeptors Antigene im Kontext mit MHCI (Haupt-Histokompatibilitäts-Komplex) erkennen und direkt cytolytisch wirken. Dies ist vor allem bei der Bekämpfung intrazellulärer Pathogene (z.B. Viren) von besonderer Bedeutung. T-Helfer-Zellen erkennen Antigen im Kontext mit MHCII und spielen eine wichtige Rolle bei der Aktivierung von B-Zellen und der Sekretion von Cytokinen. Sowohl T- als auch B-Zellen sind in der Lage, sich zu langlebigen Gedächtniszellen (immunologisches Gedächtnis) zu entwickeln, die bei einer sekundären Erkrankung mit einem bestimmten Pathogen sofort aktiv werden. Weiterhin besteht Evidenz für spezifische Suppressor-T-Lymphocyten (regulator T-cells), die, zumindest im Tiermodell, bei der Suppression der Immunantwort eine wichtige Rolle bei der Prävention von Autoimmunkrankheiten und bei der Transplantatabstoßung spielen. Lymphocyten, die weder T- noch B-Zell-Antigene exprimieren (ca. 5–10%), werden Null-Zellen genannt. Eine bedeutende Gruppe der Null-Zellen sind die sog. Natural-Killer-Zellen (NK-Zellen). Diese großen, granulären Lymphocyten können spezifische Tumortoxizität aufweisen sowie spezifisch Zellen abtöten, die MHCI aufgrund einer Virusinfektion oder Entartung „herunterreguliert" haben. Aus dem Verhältnis der einzelnen Lymphocyten-Subpopulationen zueinander lassen sich Störungen des Immunsystems, z.B. bei angeborenen Defekten (Immundefektsyndrom), Tumoren (Krebs), Infekten (z.B. AIDS, HIV-Infektion; Infektionskrankheiten), Autoimmunkrankheiten, näher charakterisieren. Von großer Bedeutung ist die T-Zell-Analyse bei der Überwachung von Patienten nach Herz-, Nieren- oder Knochenmark-Transplantationen zur Frühdiagnose von Abstoßungsreaktionen. Blutbildung, Clone-selection-Theorie, Erythrocyten, immunkompetenter Lymphocyt, Immunkompetenz, Interferone, Interleukine, Lymphocyten-Aktivierung, Lymphocyten-Mischkultur, Lymphocyten-Rezirkulation, Lymphocyten-Transformation, Lymphokine; Blutbildung .
H.N./A.F.
Lymphocyten
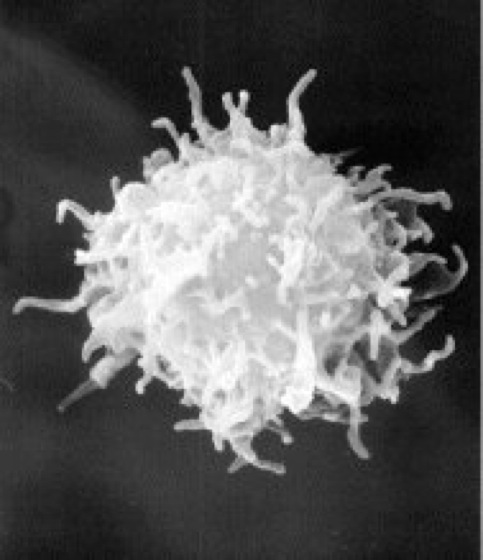
Abb. 1: Lymphocyt des Schafes in einer rasterelektronenmikroskopischen Aufnahme
Lymphocyten
Abb. 2: Vereinfachtes Schema der Lymphocyten-Wechselwirkungen (gestrichelt: stimulierende Wirkung, gepunktet: hemmende, regulierende Wirkung).
Die Anzahl der B- und T-Lymphocyten in einem Organismus verändert sich nach der Reifung des Immunsystems nicht mehr, obwohl täglich Millionen neuer Lymphocyten gebildet werden. Lange Zeit vermutete man, daß alte Lymphocyten durch die neu gebildeten ersetzt werden. In letzter Zeit haben sich aber Hinweise gehäuft, daß es nur einem Teil der neu gebildeten Lymphocyten gelingt, die alten Zellen zu ersetzen; die meisten sterben wieder ab. Nur die Lymphocyten, die gegenüber den alten Lymphocyten einen Selektionsvorteil besitzen, können sich im Immunsystem etablieren. Die meisten Lymphocyten leben nach dieser Vorstellung wochen-, monate- oder gar jahrelang. Einige von ihnen sind somit vermutlich identisch mit den Gedächtniszellen (immunologisches Gedächtnis), die bei einer Immunantwort nach dem ersten Kontakt mit dem Antigen aktiviert werden. Das Wechselspiel mit dem in den Lymphknoten gespeicherten Antigen sowie mit anderen Lymphocyten und deren Botenstoffen bestimmt, wie lange Lymphocyten leben.
Schreiben Sie uns!