Lexikon der Chemie: Lignin
Lignin, ein Biopolymer der höheren Pflanzen. L. ist neben Cellulose und den Hemicellulosen Hauptbestandteil der verholzten pflanzlichen Zellwände. Laub- und Nadelhölzer enthalten etwa 20 bis 35 % L. L. ist ein amorphes, optisch inaktives, dreidimensionales Heteropolymer, das sich unzersetzt in keinem üblichen Lösungsmittel löst. L. entsteht biosynthetisch durch oxidative Polymerisation von hydroxylierten und teilweise methoxylierten Zimtalkoholen, überwiegend des Coniferylalkohols. Je nach Herkunft variiert der Anteil der einzelnen Monomeren. Im L. der Pteridophyten und Gymnospermen überwiegen im allg. Guajacylreste (4-Hydroxy-3-methoxyphenyl-, Guajacyllignin). Das L. der Nadelhölzer enthält z. B. durchschnittlich 14 % 4-Hydroxyphenyl-, 80 % Guajacyl- und 6 % Syringyl(4-Hydroxy-3,5-dimethoxyphenyl)-reste. Das L. der Laubhölzer enthält etwa gleiche Teile Guajacyl- und Syringylreste (Guajacylsyringyllignin), jedoch kaum 4-Hydroxyphenylreste. Innerhalb der Dicotyledonen enthalten Kräuter weniger Syringylreste als verholzte Arten. Etwa 10 % 4-Hydroxyphenylreste sind im allg. im L. monocotyledoner Pflanzen enthalten. Die Monomeren werden biosynthetisch auf dem Shikimisäureweg über Phenylalanin, Zimtsäure und die entsprechend substituierten Zimtsäuren (Hydroxyzimtsäuren) gebildet. Die Polymerisation der Monomeren wird enzymatisch durch Peroxidasen eingeleitet. Es bilden sich zunächst mesomer stabilisierte Aroxylradikale. Die Polymerisation erfolgt durch nichtenzymatische Paarung der Radikale. Die Monomeren sind danach über C-C- und C-O-C-Bindungen miteinander zu einer netzwerkartigen Struktur verknüpft. Hemicellulosen sind daran über Etherbrücken gebunden. Die bevorzugten Bindungstypen des L. zeigt die Abbildung.
Die Biosynthese des L. ist als Dehydrierungspolymerisation aufzufassen, bei der die enzymatische Phenoldehydrierung und die nichtenzymatische Polymerisation miteinander gekoppelt sind. Entscheidende Enzyme sind die Laccasen (Phenoldehydrogenasen), die auch zur "künstlichen" Herstellung von L. aus Coniferylalkohol herangezogen werden können.
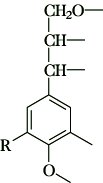
Lignin. Abb. 1: Vom Coniferylalkohol (R = OCH3) ausgehende Bindungsmöglichkeiten im Lignin.
Bei der Cellulosegewinnung aus Holz muß das L. entfernt werden. Nach industriellen Verfahren wird das Holz mit Natronlauge, der Natriumsulfid und -sulfat zugesetzt sind, gekocht – alkalisches Aufschlußverfahren oder Sulfatverfahren – oder mit Hydrogensulfitlösung behandelt - saures Aufschlußverfahren oder Sulfitverfahren (Zellstoff). Beim Sulfitverfahren entstehen niedermolekulare, wasserlösliche, biologisch schwer abbaubare Ligninsulfonsäuren oder Ligninsulfonate.

Lignin. Abb. 2: Typische Struktur des Nadelbaumlignins.
Lignin wird u. a. als Bindemittel (z. B. bei der Brikettierung und Pelletierung, zur Böschungsbefestigung) oder als Dispergiermittel (z. B. in der Zementverarbeitung, in der keramischen Industrie, als Zusatz für Bohrspülmittel) verwendet. Durch oxidativen Abbau wird Vanilin, durch nucleophilen Abbau Dimethylsulfid gewonnen.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.