Lexikon der Chemie: Massenspektrometrie
Massenspektrometrie, Massenspektroskopie, Methode zur Ermittlung der Masse und Häufigkeit geladener Teilchen. Das Prinzip der M. besteht darin, aus Atomen oder Molekülen durch geeignete Ionisationsverfahren Ionen zu erzeugen, diese nach ihrem Verhältnis Masse/Ladung (m/z) zu trennen und mit Hilfe einer Registriereinrichtung das Massenspektrum aufzuzeichnen.
Die M. dient zur Strukturaufklärung organischer und anorganischer Verbindungen zur Spurenanalyse, zur exakten Bestimmung von Atommassen und Isotopenhäufigkeiten, zur Ermittlung von Ionisierungs-, Bildungs- und Dissoziationsenergien, zur Bestimmung der Elementarzusammensetzung organischer Verbindungen, zur Untersuchung von Ionenreaktionen in der Gasphase u. a.
Apparative Grundlagen. Ein Massenspektrometer besteht aus vier Funktionsteilen (Abb. 1): dem Einlaßsystem, der Ionenerzeugung (Ionenquelle), der Ionentrennung und dem Ionennachweis.

Massenspektrometrie. Abb. 1: Schema eines Massenspektrometers.
1) Einlaßsystem. Die Probe muß sich im gasförmigen Zustand unter einem Druck von etwa 10-4 Pa befinden. Unter diesen Bedingungen liegt die mittlere freie Weglänge der Ionen zwischen 10 und 100 m, während die Weglänge im Massenspektrometer etwa 1 m beträgt. Dadurch werden Zusammenstöße zwischen den gebildeten Ionen oder Neutralteilchen vermieden, die eine exakte Massentrennung verhindern. Mit Hilfe des Einlaßsystems wird so viel Substanz in die Dampfphase übergeführt, daß der angegebene Druck in der Ionenerzeugung erreicht wird. Leicht flüchtige Stoffe werden zunächst in einem Vorratsbehälter verdampft, von wo aus sie durch eine Düse in die Ionenerzeugung strömen können. Schwerer flüchtige Substanzen, die jedoch noch ohne Zersetzung einen Dampfdruck von 10-4 Pa erreichen, werden unmittelbar in die Ionenquelle eingeführt. Unverdampfbare Substanzen können entweder durch Überführung in verdampfbare Derivate oder durch spezielle Ionisationstechniken untersucht werden (Festkörpermassenspektroskopie, s. u.).
2) In der Ionenquelle wird die Probe ionisiert, die entstandenen Ionen werden beschleunigt und zu einem Strahl gebündelt. Die Ionisation erfolgt meist durch Elektronenstoßionisation, chemische Ionisation, Feldionisation oder Photoionisation. Prinzipiell können sowohl positive als auch negative Ionen gebildet werden, die zudem noch einfach oder mehrfach geladen sein können:
Die einfach positiv geladenen Ionen treten bei allen Ionisierungstechniken jedoch am häufigsten auf und sind am meisten untersucht. Die massenspektrometrische Untersuchung negativer Ionen (Elektronenanlagerungsmassenspektrometrie) ist nur für spezielle Zwecke (z. B. Molekülmassebestimmung von Naturstoffen) bedeutend. Von den genannten Ionisierungstechniken ist die Elektronenstoßionisation am weitesten verbreitet. Aus der gasförmig vorliegenden Probe wird durch Beschuß mit Elektronen, die aus einer Glühkathode emittiert werden, ein Elektron herausgeschlagen, so daß ein positiv geladenes Ion entsteht. Die Energie der Beschußelektronen kann variiert werden, wird aber meist auf 70 eV eingestellt, da damit eine günstige Ausbeute an einfach positiv geladenen Ionen erhalten wird. Die Beschleunigung der erzeugten Ionen erfolgt durch ein Potential von einigen Kilovolt, die Fokussierung auf den Eintrittsspalt der Ionentrennung mit Hilfe elektrostatischer Linsen.
3) In der Ionentrennung werden die Ionen nach ihrem Masse/Ladungs-Verhältnis m/z mittels statischer oder dynamischer Methoden getrennt. Am häufigsten werden gegenwärtig magnetische Sektorfeldgeräte verwendet, in denen die Trennung der Ionen durch ihre Ablenkung in einem starken Magnetfeld erreicht wird (statische Methode). Mittels dynamischer Methoden erfolgt die Ionentrennung in Flugzeitmassenspektrometern, in denen die Trennung auf der massenabhängigen Geschwindigkeit der Ionen beruht, oder in Quadrupolmassenspektrometern, in denen der Ionenstrahl zwischen vier stabförmige Pole eines elektrischen Wechselfeldes gelenkt wird. Nur diejenigen Ionen, die im Takt des Wechselfeldes ihre Richtung ändern, werden vom Massenfilter durchgelassen.
4) Zum Ionennachweis benutzt man vor allem drei Typen von Empfängern: a) Im Faraday-Auffänger wird die Ladung, die die Ionen dort abgeben, über einen Hochohmwiderstand zur Erde abgeleitet. Der dabei am Widerstand entstehende Spannungsabfall ist der Ionenmenge proportional und wird nach entsprechender Verstärkung von einer geeigneten Registriereinrichtung (z. B. einem Kompensationsschreiber) gemessen. Mit Lichtpunktschreibern können die Spektren in wenigen Sekunden registriert werden. b) Im Sekundärelektronenvervielfacher bewirken die auf eine Dynode treffenden Ionen die Emission mehrerer Sekundärelektronen, die weiter verstärkt werden. c) Die Verwendung einer Photoplatte als Empfänger setzt voraus, daß die Ionen unterschiedlicher Masse in einer Ebene fokussiert werden. Die hierbei verwendeten Geräte sind die Massenspektrographen.
Da zahlreiche im Massenspektrometer anfallenden Informationen leicht digitalisiert werden können, setzt sich die direkte Kopplung von Massenspektrometern mit Computern (computerintegrierte Systeme) zur Auswertung und Gerätesteuerung immer mehr durch.
Darstellung der Massenspektren. Da in einem Massenspektrum Peaks extrem unterschiedlicher Intensität auftreten können, ist es häufig notwendig, Schreiber mit abgestuften Empfindlichkeitsbereichen (z. B. 1 : 10 : 100) zu verwenden. Da derartig registrierte Spektren recht unübersichtlich sind, ist es üblich, Massenspektren zum Zwecke der Bearbeitung und Lagerung entweder in Form von Tabellen oder von Strichspektren wiederzugeben. In einem Strichspektrum trägt man die m/z-Werte der Ionen gegen ihre relative Häufigkeit auf, wobei der intensivste Peak, der Basispeak, willkürlich gleich 100 % gesetzt wird (Abb. 2).
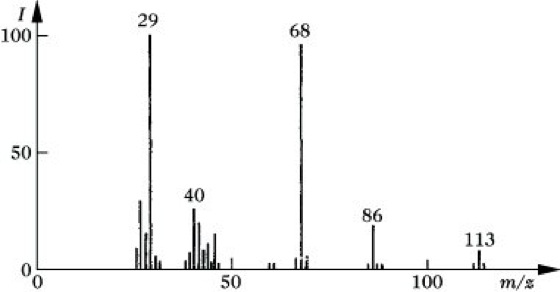
Massenspektrometrie. Abb. 2: Massenspektrum von Cyanessigsäureethylester
Anwendung der M. 1) Strukturaufklärung. Die M. kann Aussagen zur relativen Molekülmasse, zur Summen- und zur Strukturformel einer Verbindung liefern. Da Moleküle fast ausnahmslos eine gerade Anzahl von Elektronen enthalten, bildet sich bei ihrer Ionisierung durch Herausschlagen eines Elektrons ein Radikalkation mit einem ungepaarten Elektron M+. Dieser Prozeß der Molekülionenbildung setzt ein, sobald die Elektronenstoßenergie der Ionisationsenergie des Moleküls entspricht, die auf diese Weise bestimmt werden kann. Die Ionisationsenergien von Molekülen liegen im allg. zwischen 6 und 15 eV. Wird bei einem Stoßprozeß mehr Energie übertragen, als zur Ionisierung notwendig ist, so tritt ein teilweiser Zerfall des Moleküls in Bruchstücke (Fragmente) auf. Die Fragmentierung des Molekülions sowie weiterer daraus gebildeter Ionen erfolgt so, daß Ionen mit ungerader Elektronenzahl in Radikale und Teilchen mit gerader Elektronenzahl – dies können Ionen oder Neutralteilchen sein – zerfallen, während Ionen mit gerader Elektronenzahl wieder Teilchen mit gerader Elektronenzahl bilden: M+· → A+ + R· , M+· → B+· + N, A+ → C+ + N.
Zur Bildung von Fragmentionen ist eine Mindestenergie, die Auftrittsenergie, erforderlich. Sie übersteigt die Ionisierun:senergie um die Dissoziationsenergie der gesprengten Bindung. Die bei der Fragmentierung entstehenden ungeladenen Bruchstücke (Radikale und Neutralteilchen) werden durch die das Vakuum erzeugenden Diffusionspumpen aus dem Massenspektrometer entfernt.
Molekülmassebestimmung. Der Peak des einfach ionisierten Moleküls (Molekülpeak) M+· ist meist der letzte größere Peak im Massenspektrum, der nur noch von Isotopenpeaks bei M +1, M +2 oder auch noch höheren Massen begleitet wird. Er liefert, sofern er eindeutig erkannt werden kann, die relative Molekülmasse der untersuchten Verbindung. In einfach fokussierenden Massenspektrometern erfolgt diese Bestimmung auf eine Masseneinheit (Nominalmasse) genau. So kann bei niedriger Auflösung zwischen den Ionen CO+·, N2+· oder C2H4+·, für die alle m/z ≈ 28 ist, nicht unterschieden werden. Bei höherer Auflösung, wie sie in doppelfokussierenden Geräten erfolgt, und der damit möglichen genaueren Massenbestimmung auf 4 Dezimalen (Feinmassenbestimmung) ist dies möglich (CO· 27,9949, N2+· 28,0062, C2H4+· 28,0312), so daß aus diesem genaueren Wert auch die Bruttoformel der vermessenen Verbindung bestimmt werden kann. Schwierigkeiten bei der Erkennung des Molekülpeaks können auftreten, wenn das Molekülion sehr instabil ist und schnell weiter zerfällt, so daß es nur mit sehr geringer Intensität oder gar nicht im Massenspektrum erscheint.
Isotopenpeaks und Summenformel. Molekülpeaks (und auch Fragmentpeaks) sind im Massenspektrum häufig von Peaks geringerer Intensität, den Isotopenpeaks, begleitet. Sie entstehen dadurch, daß die meisten in Molekülen enthaltenen Elemente aus mehreren Isotopen bestehen (Tab. 1). Das Isotopenverhältnis der Elemente bestimmt das Intensitätsverhältnis dieser Peaks. So weisen alle einfach geladenen Ionen, die Kohlenstoff enthalten, einen um eine Masseneinheit höheren Isotopenpeak auf, der vom natürlichen Gehalt an 13C (1,1 %) im Kohlenstoff herrührt. Die Intensität dieses Peaks ergibt sich für ein Ion mit n C-Atomen zu n · 1,1 % des 12C-Peaks. So erscheint im Massenspektrum des Benzens neben dem Molekülpeak bei m/z = 78 der Isotopenpeak bei m/z = 79, der eine Intensität von 6,6 % des 12C-Peaks ausmacht. Weitere typische Isotopenpeaks, die allerdings um 2 Masseneinheiten höher als der Molekülpeak auftreten, ergeben Chlor, Brom und Schwefel (Tab. 1). Es lassen sich somit aus den Isotopenpeaks Aussagen über die Anwesenheit und die vorhandene Anzahl bestimmter Elemente machen, die wichtige Anhaltspunkte zum Aufstellen der Summenformel geben, sofern diese nicht durch hochauflösende M. bestimmt werden kann. Aussagen über die Anwesenheit von Stickstoff können aus der Isotopenverteilung nicht gemacht werden, dafür aber aus der Stickstoffregel, nach der Moleküle mit einer ungeraden Anzahl von N-Atomen eine ungeradzahlige Molekülmasse aufweisen.
Massenspektrometrie. Tab. 1 Natürliche Isotopenverteilung und relative Atommasse einiger für die M. wichtiger Elemente.
| ||||
| 1H | 99 | ,985 | 1,007825 | |
| 2H | 0 | ,015 | 2,014102 | |
| 12C | 98 | ,9 | 12,000000 | |
| 13C | 1 | ,1 | 13,003354 | |
| 32S | 95 | ,0 | 31,972074 | |
| 33S | 0 | ,76 | 32,971461 | |
| 34S | 4 | ,2 | 33,967865 | |
| 35Cl | 75 | ,8 | 34,968855 | |
| 37Cl | 24 | ,2 | 36,965896 | |
| 79Br | 50 | ,5 | 78,918348 | |
| 81Br | 49 | ,5 | 80,916344 |
Strukturformel.Rückschlüsse auf die Struktur einer Verbindung sind aus dem Massenspektrum deshalb möglich, weil gewisse Regelmäßigkeiten der Fragmentierung in Abhängigkeit von der Struktur bekannt sind. Bevorzugt laufen solche Fragmentierungen ab, die energetisch begünstigt sind. So bilden sich z. B. bevorzugt solche Fragment-Ionen wie das Tropylium-Ion oder das tert-Butyl-Kation, in denen die positive Ladung durch mesomeren oder induktiven Effekt stabilisiert ist, oder solche, deren Bildung durch Eliminierung eines energiearmen Neutralteilchens (z. B. CO oder HCN) energetisch vorteilhaft ist. Weiterhin spielt die Stärke der bei der Fragmentierung aufzubrechenden Bindung eine wesentliche Rolle. So werden C-C-Bindungen leichter als C-H-Bindungen gespalten. Diese und andere Regelmäßigkeiten sind in einer Reihe mehr oder weniger empirischer Fragmentierungsregeln niedergelegt, die zur Strukturaufklärung herangezogen werden müssen. Neben einfachen Fragmentierungen, in denen im ursprünglichen Molekül bereits vorhandene Bindungen aufgebrochen werden, sind häufig Fragmentierungen mit Umlagerungen verbunden, die zu Bruchstücken führen, die im ursprünglichen Molekül nicht vorhanden waren. So findet man z. B. im Massenspektrum des Isobutans (CH3)2CH-CH3 einen Peak für das Ethylkation C2H5+, das erst durch Umlagerung entstanden ist. Bei der Auswertung eines Massenspektrums zur Strukturaufklärung ist zunächst auf Bruchstücke im niederen Massenbereich (Schlüsselbruchstücke) zu achten, die oft Hinweise auf das Vorhandensein bestimmter Strukturelemente geben (Tab. 2). So ist z. B. das Auftreten des Ions CH2=OH+ mit der Massenzahl 31 typisch für Alkohole und Ether. Im höheren Massenbereich können aus den Massendifferenzen zwischen zwei Peaks die Massen der abgespaltenen Radikale oder Neutralteilchen entnommen werden (Tab. 3). Die aus den Schlüsselbruchstücken und Massendifferenzen abgeleiteten Informationen reichen meist zur Aufstellung eines Strukturvorschlages aus. Anhand bekannter Fragmentierungsregeln muß dann überprüft werden, ob die für die postulierte Struktur zu erwartende Fragmentierung zu dem experimentell gefundenen Massenspektrum führen kann (Abb. 2 und 3).
Massenspektrometrie. Tab. 2: Wichtige Schlüsselbruchstücke.
| |||
| 29 | (C2H5)+ | Alkylgruppen | |
| 30 | (NO)+ | Nitroverbindungen | |
| 30 | (CH2=NH2)+ | Amine | |
| 31 | (CH2=OH)+ | Alkohole, Ether | |
| 39 | (C3H3)+ | Aromaten | |
| 43 | (C3H7)+ | Alkylgruppen | |
| 43 | (CH3CO)+ | Acetylgruppen | |
| 45 | (COOH)+ | Carbonsäuren | |
| 51 | (C4H3)+ | Aromaten | |
| 57 | (C4H9)+ | Alkylgruppen | |
| 59 | (COOCH3)+ | Methylester | |
| 77 | (C6H5)+ | Aromaten |
Massenspektrometrie. Tab. 3: Charakteristische Massendifferenzen M – X zwischen Molekül und Fragment-Ion.
| |||
| M – 16 | O | Nitroverbindungen Sulfoxide | |
| M – 16 | NH2 | Amide | |
| M – 17 | OH | O-haltige Verbindungen | |
| M – 17 | NH3 | Aminoverbindungen | |
| M – 18 | H2O | Alkohole, Ketone | |
| M – 26 | C2H2 | Aromaten | |
| M – 27 | HCN | Nitrile, N-Heterocyclen | |
| M – 28 | CO | Arylketone, Chinone | |
| M – 29 | C2H5 | Alkylverbindungen | |
| M – 30 | NO | Nitroaromaten | |
| M – 26 | HCl | Chlorverbindungen | |
| M – 44 | CO2 | Ester, Anhydride |
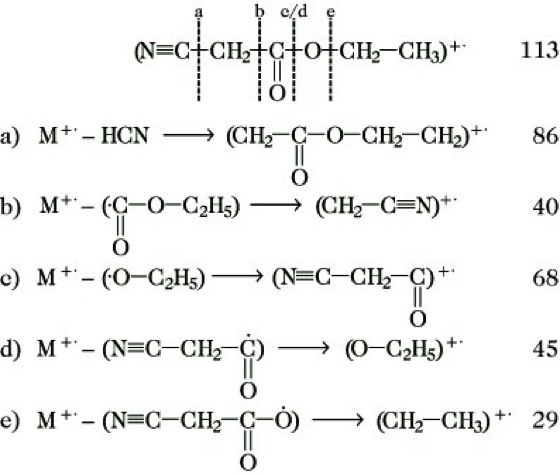
Massenspektrometrie. Abb. 3: Fragmentierungsschema von Cyanessigsäureethylester.
Die Aufstellung der Strukturformel kann häufig durch die Peaks metastabiler Ionen erleichtert werden, d. s. solche, die auf ihrer Flugbahn im Massenspektrometer im feldfreien Raum zwischen Ionenerzeugung und Ionennachweis weiter zerfallen. Sie werden im Massenspektrum nicht mehr als scharfe Linien mit der Masse des Ausgangsions registriert, sondern als breite Peaks mit geringer Intensität bei der scheinbaren Masse m* = m22/m1 wobei m1 die Masse des Ausgangs-Ions, m2 die Masse des Zerfalls-Ions ist. Das Auftreten metastabiler Ionen kann als Beweis für eine Einschrittfragmentierung von m1 nach m2 angesehen werden.
In neuerer Zeit gewinnen Meßmethoden (DADI, Abk. von engl. direct analysis of daughter ions, oder MIKES, Abk. von engl. mass analyzed ion kinetic energy spectrometry) steigende Bedeutung, die es gestatten, den weiteren Zerfallsweg eines bestimmten metastabilen Ions zu verfolgen. Dies ist mit modifizierten hochauflösenden Massenspektrometern möglich, in denen man mit Hilfe des magnetischen Analysators ein bestimmtes metastabiles Ion herausfiltert und dessen weiteren Zerfall im elektrostatischen Analysator verfolgt. Bestrebungen, diesen Typ der M. durch Hinzufügen eines dritten oder sogar vierten Analysators weiter zu verbessern (MS/MS), gehen weiter.
2) Als Mikro- und Spurenmethode, mit der noch Substanzmengen im Nanogrammbereich und Konzentrationsunterschiede bis 1 : 106 direkt erfaßt werden können, ist die M. für die qualitative und quantitative Analyse von großer Bedeutung. Die qualitative Analyse beruht auf dem Vergleich des Massenspektrums der Probe mit einer Vergleichsprobe, wobei auf konstante apparative Bedingungen geachtet werden muß. Die quantitative massenspektroskopische Analyse beruht auf der Proportionalität des gemessenen Ionenstroms, der z. B. in Form der Peakhöhe gemessen wird, mit dem Partialdruck der Probe in der Ionenquelle. Es wird die Intensität eines Peaks der Probe mit dem eines Standards (äußerer oder innerer Standard) verglichen.
Bei Gemischen setzt sich die Peakhöhe I bei der Massenzahl k additiv aus Beiträgen der einzelnen Komponenten zusammen, so daß auch Gemischanalysen durchgeführt werden können: Ik = Σ Eikpi. Dabei ist Eik der Eichwert der Komponente i bei der Massenzahl k und pider Partialdruck der Komponente i. Mit n Gleichungen dieser Form für n verschiedene Massen können n unbekannte pi berechnet werden.
Die massenspektrometrische Analyse wird außer in der reinen Chemie auch in der Biochemie, klinischen Chemie, Toxikologie, im Umweltschutz und anderen Gebieten angewendet, wobei meist Probleme der Spurenbestimmung im Vordergrund stehen. Weite Verbreitung hat die M. auch zur Bestimmung komplizierter Substanzgemische gefunden, z. B. in der Kohlenwasserstoffanalytik. Hier steht in vielen Fällen nicht die Bestimmung einzelner Individuen, sondern die Gruppenanalyse im Vordergrund.
3) Festkörpermassenspektrometrie. Während mit den bisher beschriebenen Techniken gasförmige oder verdampfbare Proben ionisiert wurden, wird der Zweig der M., der sich mit der Bildung gasförmiger Ionen aus nichtflüchtigen, vornehmlich anorganischen Festkörpern, wie Metallen, Halbleitern, Mineralen, und ihrer massenspektrometrischen Untersuchung beschäftigt, als Festkörpermassenspektrometrie bezeichnet. Eine solche Abgrenzung scheint gerechtfertigt, da zur Freisetzung und Ionisierung der Atome oder Moleküle aus dem Festkörperverband spezielle Ionenquellen erforderlich sind. Herkömmliche Techniken sind die thermische Ionisierung, die bei hohen Temperaturen zur Freisetzung von Ionen aus anorganischen Festkörpern führt, und die Funkenionisierung, bei der die Ionenbildung durch Abfunken der zu analysierenden Probe, die sich in einer der beiden Elektroden befindet, erfolgt. In der Sekundärionenmassenspektrometrie (Abk. SIMS) werden in einer Primärionenquelle aus einem reinen Gas (Edelgase oder Sauerstoff) Ionen erzeugt, die anschließend beschleunigt und auf eine Probe fokussiert werden. Durch diesen Ionenbeschuß werden Sekundär-Ionen ausgelöst, die im Massenspektrometer untersucht werden. Bei der Lasermassenspektrometrie wird Laserlicht zur Ionisierung und Verdampfung von Festkörperproben benutzt. Bei der Felddesorptionsmassenspektrometrie wird die zu untersuchende Probe direkt auf die Anode gebracht. Durch Anlegen eines starken elektrischen Feldes werden positive Ionen von der Anode ausgestoßen.
4) Spezielle Anwendungen. Durch Kopplung mit der Gaschromatographie (GC/MS-Kopplung) konnte die M. wesentlich erweitert werden. Dabei werden die in einem Gaschromatographen getrennten Komponenten eines Substanzgemisches mit einem Massenspektrometer, das direkt mit dem Gaschromatographen verbunden ist, analysiert, sobald sie die chromatographische Säule verlassen haben. Die Identifizierung sehr kleiner, in einem Gemisch vorliegender Substanzmengen (bis in den ppb-Bereich) ist die wichtigste Anwendung dieser Methode. Auch die Kopplung der Flüssigchromatographie mit der Massenspektrometrie (LC/MS-Kopplung) wird angewandt. Besonders zur Untersuchung von Hochpolymeren hat sich die Pyrolysemassenspektrometrie bewährt. Die Hochpolymeren werden zunächst pyrolisiert und ihre Bruchstücke massenspektrometrisch untersucht. Die M. ist auch zur Elementspurenanalytik geeignet: Bei der ICP-MS wird ein induktiv gekoppeltes Plasma verwendet, um Ionen zu erzeugen, die massenspektrometrisch analysiert werden.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.