Lexikon der Chemie: Mutterkornalkaloide
Mutterkornalkaloide, Secalealkaloide, Verbindungen, die das Ergolin-Grundgerüst enthalten und von Claviceps purpurea und einigen anderen Pilzen gebildet werden. Als Mutterkorn (Secale cornutum) bezeichnet man die Dauerform (Sklerotium) des auf Gramineen, insbesondere auf Roggen, parasitierenden Pilzes. Bisher sind über 30 M. bekannt geworden.
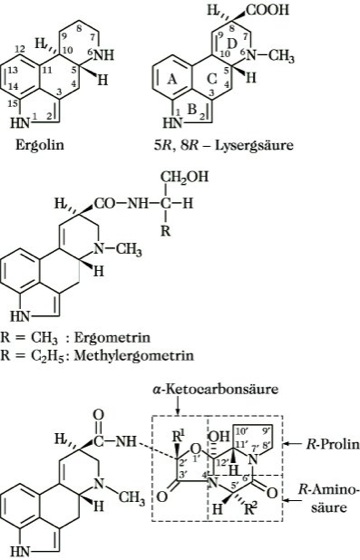
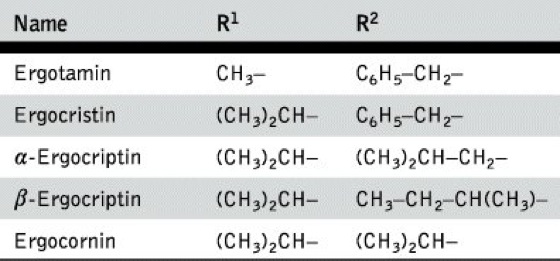
Biosynthese. Die Biosynthese der Verbindungen erfolgt aus der Aminosäure Tryptophan und einem aktivierten Derivat des Isoprens. Dabei entstehen zunächst Alkaloide vom Clavin-Typ (Clavinalkaloide), die vor allem am Piperidinring keine Carboxygruppe, sondern eine Methylgruppe oder eine Hydroxymethylgruppe enthalten bzw. bei denen der Piperidinring noch nicht geschlossen ist. Diese Verbindungen spielen als Arzneimittel keine Rolle. Die Oxidation der Methyl- bzw. Hydroxymethylgruppe am C-Atom 8 führt zur 5R,8R-Lysergsäure (D-Lysergsäure), die charakteristischer Bestandteil der therapeutisch verwendeten M. ist. Man unterscheidet M., bei denen die Carboxygruppe der Lysergsäure mit einem niedermolekularen Aminoalkohol säureamidartig verknüpft ist (Ergometringruppe), und M., bei denen in gleicher Weise ein cyclischer Peptidrest gebunden ist (Ergotamingruppe, Ergotoxingruppe). Verbindungen der Ergometringruppe werden auch als wasserlösliche M. von den als wasserunlösliche M. bezeichneten Peptidalkaloiden unterschieden. Verbindungen der Ergotamingruppe enthalten als gemeinsamen Aminosäurebaustein im Peptidteil D-Alanin und Verbindungen der Ergotoxingruppe D-Valin. Am Aufbau des cyclischen Peptidteils sind bei den entsprechenden M. außerdem D-Prolin, eine weitere D-Aminosäure und eine Ketocarbonsäure beteiligt. Die meisten natürlichen M. der Ergometrin-, Ergotamin- und Ergotoxingruppe sind stark linksdrehende Verbindungen (Tab.). Durch Isomerisierung am C-Atom 8 des Lysergsäureanteils, durch den die Konfiguration der 5R,8S-Isolysergsäure (D-Isolysergsäure) erhalten wird, entstehen stark rechtsdrehende Verbindungen, die durch Anhängen der Silbe "in" an den Namen des natürlichen M. bezeichnet werden, wie z. B. Ergometrinin und Ergotaminin. Derivate der 5R,8S-Isolysergsäure sind physiologisch unwirksam. Diese Isomerisierung erfolgt leicht, weil bei den Verbindungen in Nachbarstellung zur Carbonylgruppe des Lysergsäurerestes eine Doppelbindung im Piperidinring enthalten ist. Bei den Peptidalkaloiden erfolgt im sauren Milieu durch Isomerisierung am C-Atom 2' Bildung der physiologisch unwirksamen Aci-Alkaloide. Unter Lichteinwirkung in saurer Lösung wird an die Doppelbindung zwischen C-Atom 9 und C-Atom 10 Wasser zu den Lumi-Alkaloiden addiert. Dabei wird die OH-Gruppe am C-Atom 10 gebunden.
Mutterkornalkaloide. Tab.: Beispiele.
| ||||
| Ergometrin - Ergometrinin | 162 196 | +90° +414 | (H2O) | |
| Ergotamin - Ergotaminin | 212 242 | -160° +369° | (Chloroform) | |
| Ergocristin - Ergocristinin | 156 226 | -180° +366° | (Chloroform) | |
| Ergocornin - Ergocorninin | 183 228 | -186° +400° | (Chloroform) |
Gewinnung. Der Alkaloidgehalt der Wilddroge liegt zwischen 0 und 1 %, meist unter 0,2 %. Die Gewinnung der M. erfolgt durch Extraktion aus Sklerotien von gezüchteten Hochleistungsstämmen, die ein Alkaloid oder eine Alkaloidgruppe in möglichst hoher Konzentration bilden. Dazu wird Roggen künstlich infiziert. Die Züchtung des Pilzes auf künstlichem Nährboden ist ebenfalls möglich. Bedeutung gewinnt auch die Partialsynthese. Dabei wird von der der Lysergsäure isomeren Paspalsäure mit einer Doppelbindung zwischen C-Atom 8 und C-Atom 9 ausgegangen, die durch Submerskultur von Claviceps paspali gewonnen wird. Paspalsäure wird zu 5R,8R-Lysergsäure isomerisiert und diese über ein geeignetes reaktives Carbonsäurederivat z. B. mit einem Aminoalkohol verknüpft. Dabei kann durch Einsatz von S-2-Aminobutan-1-ol das nicht natürlich vorkommende Methylergometrin gewonnen werden. Bei analoger Umsetzung mit Diethylamin entsteht LSD. Durch Hydrierung der Doppelbindung zwischen C-Atom 9 und C-Atom 10 werden die Dihydro-M. erhalten, die wesentlich stabiler gegenüber einer Isomerisierung am C-Atom 8 sind. Durch Bromierung von α-Ergocriptin am C-Atom 2 entsteht Bromocriptin.
Alkaloide der Ergotamin- und Ergotoxingruppe bewirken als α-Sympathikolytika Gefäßerweiterung und Blutdrucksenkung, die bei den Dihydroderivaten deutlicher zutage tritt. Entsprechende M. werden unter anderem zur Migränebehandlung eingesetzt. Ergometrin (Ergobasin) hat keine α-sympathikolytischen Wirkungen. Es greift wie Methylergometrin direkt am Uterus an und ruft in niedriger Konzentration Tonuserhöhung und rhythmische Kontraktionen hervor. Es wird hauptsächlich nach der Geburt zur Lösung der Plazenta und zur Blutstillung verwendet. Bromocriptin hemmt die Prolactinausschüttung und kann damit zum Abstillen eingesetzt werden. Als Dopamin-Agonist kann es außerdem als Antiparkinsonmittel verwendet werden.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.