Lexikon der Chemie: Raman-Spektroskopie
Raman-Spektroskopie, Teilgebiet der Spektroskopie, das auf dem Raman-Effekt beruht. Dieser basiert auf der Erscheinung, daß sich im Streuspektrum von mit monochromatischem Licht bestrahlten Molekülen Linien befinden, deren Frequenzen sich von der des eingestrahlten Lichtes unterscheiden. Sie rühren von Molekülschwingungen und Molekülrotationen her.
Entstehung des Raman-Spektrums. Wird eine Probe intensiv mit einer monochromatischen Strahlung der Frequenz ν0 bestrahlt, die weit genug von einer Absorptionsstelle der Substanz entfernt ist, so wird ein Teil des auffallenden Lichtes gestreut (Abb. 1).

Raman-Spektroskopie. Abb. 1: Streustrahlung als Urspung des Raman-Spektrums.
Die Streuintensität ist proportional ν4, so daß eine Strahlung nur bei Verwendung von sichtbarem und ultraviolettem Licht beobachtet wird. Die spektrale Zerlegung des gestreuten Lichtes in einem Spektrometer zeigt, daß darin vorwiegend die Erregerfrequenz ν0(Rayleigh-Streustrahlung), jedoch außerdem noch weitere Frequenzen (Raman-Streustrahlung) vorhanden sind. Diese Frequenzen (Raman-Linien) sind symmetrisch unterhalb und oberhalb der Rayleigh-Linie (Erreger-Linie) angeordnet (Abb. 2).

Raman-Spektroskopie. Abb. 2: Abstand der Stokesschen und Anti-Stokesschen Linien im Streuspektrum des Kohlenstofftetrachlorids von der Erregerlinie.
Die Frequenzdifferenzen Δν der Raman-Linien zur Rayleigh-Linie entsprechen den Schwingungsfrequenzen νsdes Moleküls. Die Raman-Linien, die eine kleinere Frequenz bzw. Wellenzahl als die Erregerlinie haben und somit energieärmer sind, werden Stokessche Linien genannt. Sie entstehen, indem Moleküle, die sich im Schwingungsgrundzustand befinden, aus der Erregerstrahlung Energie aufnehmen und in einen angeregten Schwingungszustand übergehen (Abb. 3a). Die Differenz zwischen Erregerlinie und Raman-Linie entspricht somit der Schwingungsfrequenz. Bereits in einem angeregten Schwingungszustand befindliche Moleküle können diese Anregungsenergie bei der Wechselwirkung mit der Erregerstrahlung abgeben. Dabei entstehen die Anti-StokesschenLinien, die eine höhere Frequenz bzw. Wellenzahl als die Erregerlinie aufweisen (Abb. 3b). Da die meisten Moleküle sich im Schwingungsgrundzustand befinden, ist die Intensität der Stokesschen Linien größer als die der Anti-Stokesschen.
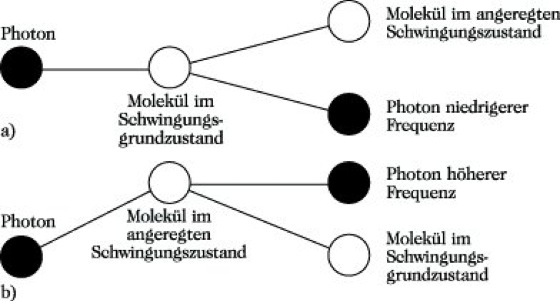
Raman-Spektroskopie. Abb. 3: Entstehung von Stokesschen (a) und Anti-Stokesschen (b) Linien.
Das Raman-Spektrum einer Substanz erhält man, wenn man die Abstände der einzelnen Raman-Linien von der Erregerlinie – meist in Wellenzahlen ausgedrückt – in Abhängigkeit von ihrer Intensität aufträgt. Die mit der R. beobachteten Wellenzahldifferenzen sind unabhängig von der verwendeten Erregerfrequenz. Sie entsprechen den bei der Infrarotspektroskopie aus den Lagen der Absorptionsbanden im IR erhaltenen Wellenzahlen. Raman-Spektrum und IR-Spektrum sind deshalb vergleichbar, aber nur teilweise identisch, was auf unterschiedliche Anregungsbedingungen zurückzuführen ist. Ebenso wie die Anregung von Molekülschwingungen im IR an bestimmte Auswahlregeln gebunden ist, gilt dies auch für den Raman-Effekt. Nur diejenigen Schwingungen, die zu einer Änderung der Polarisierbarkeit α der Elektronenhülle führen, sind Raman-aktiv und werden im Raman-Spektrum beobachtet. δα/δr ≠ 0 Raman-aktiv; δα/δr = 0 Raman-inaktiv; hierbei ist r der Abstand der Atome. Dadurch können im Raman-Spektrum Schwingungen untersucht werden, die im IR-Spektrum nicht auftreten und umgekehrt. Andere Schwingungen können sowohl Raman- als auch IR-aktiv oder -inaktiv sein. Aus der Verteilung der Eigenschwingungen eines Moleküls auf das IR- und Raman-Spektrum lassen sich Rückschlüsse auf die Molekülsymmetrie ziehen. In Molekülen mit Symmetriezentrum kann z. B. eine Schwingung nur IR- oder nur Raman-aktiv sein (Alternativverbot). Deshalb müssen IR-Spektroskopie und R. miteinander kombiniert werden, wenn das Schwingungsverhalten eines Moleküls vollständig untersucht werden soll. Neben der Frequenz und Intensität ist in der R. der Depolarisationsgrad p wichtig. Bei der Verwendung von Laser-Lichtquellen, die polarisiertes Licht emittieren, wird nach der Probe ein Polarisator geschaltet, und für jede Linie wird die Intensität I einmal bei einer parallelen Einstellung des Polarisators zur Schwingungsebene der Strahlung, zum anderen bei senkrechter Einstellung gemessen. Der Depolarisationsgrad ergibt sich zu ![]()
. Er ist wichtig zur Beschreibung der Symmetrie von Schwingungen. Für totalsymmetrische Schwingungen in isotropen Molekülen (z. B. Kohlenstofftetrachlorid CCl4) ist p= 0, für weniger symmetrische Schwingungen kann ein Wert von p = 0,75 erreicht werden.
Apparatives. Raman-Spektren können von transparenten, optisch leeren, nicht fluoreszierenden Proben, vor allem von Flüssigkeiten und Lösungen, etwas schwieriger aber auch von Gasen und Festkörpern, erhalten werden. In modernen Geräten werden zur Aufnahme eines Spektrums im Gegensatz zu älteren Spektrometern nur Milligramm-Mengen der Substanz benötigt.
Das in der R. untersuchte Streulicht ist relativ intensitätsschwach. So weist die Rayleigh-Streustrahlung etwa 10-3 der Intensität der Erregerstrahlung, die Raman-Streustrahlung etwa 10-6 bis 10-7 davon auf. Die Lichtquellen müssen deshalb sehr intensive Strahlung aussenden, ein maximaler Betrag der Streustrahlung muß gesammelt werden, und der Empfänger muß möglichst empfindlich sein. Raman-Spektrometer sind Einstrahlgeräte, die die Intensität des gestreuten Lichtes direkt messen.
Während früher ein Quecksilberbogen als Lichtquelle verwendet wurde, konnten entscheidende Verbesserungen durch den Einsatz von Lasern, kombiniert mit Sekundärelektronenvervielfachern als Empfänger, erzielt werden. Es werden Laser mit unterschiedlichen Frequenzen sowie auch durchstimmbare Laser verwendet.
Anwendung. Bedingt durch die apparative Entwicklung, wird die R. in neuerer Zeit stärker in der Chemie eingesetzt. Sie bietet innerhalb der vorgegebenen Auswahlregeln grundsätzlich die gleichen Anwendungsmöglichkeiten wie die Infrarotspektroskopie, so daß hier vor allem ihre Vor- und Nachteile gegenüber dieser Methode herausgestellt werden sollen. Die in der R. benutzten Glas- oder Quarzküvetten lassen im Gegensatz zu den Alkalihalogenidküvetten der IR-Spektroskopie eine Untersuchung aller Lösungsmittelsysteme (wäßrige, saure, alkalische Lösungen) zu, was besonders bei der Untersuchung biologischer Systeme (z. B. wäßrige Lösungen von Aminosäuren, Untersuchung von Körperflüssigkeiten oder wäßriger Lösungen anorganischer Salze) wichtig ist. Moderne Raman-Spektrometer erlauben die Erfassung sehr niedriger Absorptionsfrequenzen (unter 250 cm-1), die mit den üblichen IR-Spektrometern nicht vermessen werden können und besondere Geräte für das ferne IR erfordern. Aufgrund der unterschiedlichen Auswahlregeln ergibt das Raman-Spektrum mehr Aussagen über die Gerüstschwingungen. eines Moleküls, während im IR-Spektrum die Schwingungen polarer Gruppen besonders intensiv auftreten. Das Raman-Spektrum ist oft übersichtlicher als das IR-Spektrum, da Kombinations- und Oberschwingungen weitgehend fehlen. Für die Strukturaufklärung erweist es sich als sehr nützlich, daß manche wichtige Molekülschwingungen, die IR-inaktiv bzw. von sehr geringer IR-Intensität sind, erst im Raman-Spektrum deutlich zu erkennen sind. Das gilt z. B. für symmetrisch substituierte C=C- und C≡C-Bindungen, über die im IR-Spektrum keine Aussagen gemacht werden können. Es besteht ein linearer Zusammenhang zwischen der Anzahl der streuenden Moleküle und der Intensität der Lichtstreuung, der zu quantitativen Messungen verwendet werden kann. Da es einen beträchtlichen Aufwand erfordert, absolute Streuintensitäten zu bestimmen, so sind bei den meisten quantitativen Messungen relative Streuintensitäten ermittelt worden, aus denen z. B. mit Hilfe einer Eichkurve quantitative Analysenergebnisse erhalten werden können.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.