Eine Alternative zu Antibiotika: Phagen jagen
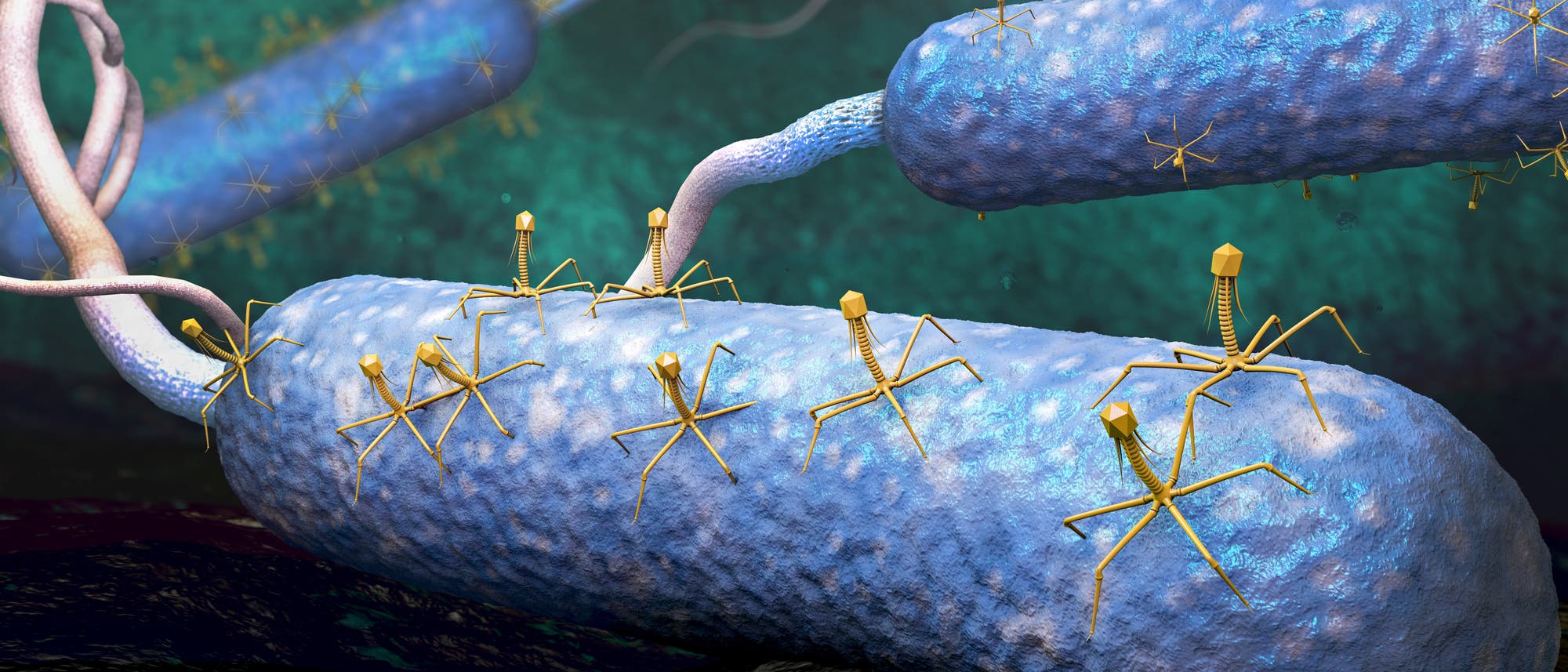
Steffanie Strathdee hätte nie gedacht, dass ein Bakterium ihre Welt einstürzen lassen würde. Sie, die Spezialisten für Infektionskrankheiten und Kodekanin eines Instituts für Globale Gesundheit an der renommierten University of California San Diego (UCSD). »Viren ja«, sagt sie, »aber Bakterien?« Im Februar 2016 kämpfte Strathdees Ehemann auf der Intensivstation der Klinik ihrer Universität mit einem ganz besonders resistenten Vertreter des Erregers Acinetobacter baumanii. Antibiotika zeigten kaum noch eine Wirkung. Extensiv drug resistent (XDR) heißt es, wenn die Grenze von multiresistent bereits überschritten ist. Von dort aus ist es nicht mehr weit zu PDR, »pan drug resistent«. Das ist – wenn man so will – die wissenschaftliche Bezeichnung für: »Da geht nichts mehr.« Dass ihr Mann dieses Stadium tatsächlich schon erreicht hat, begreift Strathdees, als sie eine Frage hört, die nicht für ihre Ohren bestimmt ist: »Hat irgendwer Steff gesagt, dass ihr Mann sterben wird?«
»Steff«, wie sie von Freunden und Kollegen genannt wird, rebelliert. Sie will sich damit nicht abfinden und beginnt zu suchen, sichtet Studien, recherchiert im Internet über »Alternativen zu Antibiotikabehandlungen«. Dort stößt sie auf eine Therapie aus Georgien, die angeblich Wunder wirken soll: Phagen, also Viren, die ausschließlich Bakterien befallen. Sie sollen bereits etliche Menschen von resistenten Keimen befreit haben. Von Phagen hatte Strathdee zuletzt im Studium gehört. Es gibt zwei unterschiedliche Sorten: Solche, die Bakterien unterstützen, und solche, die Bakterien töten. Die, über die sie aufgeregt recherchiert, sind Bakterienkiller. Sie docken an die Zellwände von Bakterien und impfen sie mit ihrer DNA, ändern also deren Erbgut. Die Bakterien werden dadurch sozusagen umprogrammiert, so dass sie in ihrem Inneren massenhaft neue Phagen produzieren. Mit Hilfe eines Enzyms lösen die Phagen von innen die Zellwand der Bakterien auf, bis diese schließlich platzen und ein Heer neuer Phagen entlassen. Das geschieht so lange, bis alle Bakterien, gegen die sich die Phagen richten, zerstört sind.
Bereits im Jahr 1917 beschrieb der französisch-kanadische Biologe Felix d’Hérelle die winzigen Killermaschinen, als sie die von ihm angelegten Bakterienkulturen zerstörten. Er nannte sie Bakteriophagen, Bakterienfresser, und hoffte damit einen Wirkstoff gegen die damals so gefährlichen Infektionen wie Wundstarrkrampf, Lungenentzündung oder Blutvergiftung gefunden zu haben. Und tatsächlich: Zwei Jahre später heilte er so den ersten Patienten. Neun Jahre bevor Alexander Fleming das Penizillin entdeckte. Mit seinem Freund und Kollegen Georgi Eliava gründet er im Jahr 1933 das erste Institut für Phagenforschung in Tiflis, der Hauptstadt Georgiens, das mittlerweile Eliava-Institut heißt.
Doch mit Entwicklung der ersten Antibiotika in den 1940er Jahren kommt die Phagenforschung fast vollständig zum Erliegen. Die Bakterienkiller haben einen aus damaliger Sicht entscheidenden Nachteil: Sie sind hochspezifisch, das heißt, sie bekämpfen stets nur eine Bakterienart, manchmal lediglich einen einzigen Stamm. Bei Infektionen muss also zunächst der genaue Erreger bestimmt und dann nach den richtigen Phagen gesucht werden. Das nimmt wertvolle Zeit in Anspruch. Antibiotika hingegen wirken sofort und machen keine Unterschiede, wen sie töten.
Der Penizillin-Entdecker Fleming warnte zwar bereits in seiner Rede zum Nobelpreis, den er im Jahr 1945 für seine Entdeckung erhielt, dass die Wundermittel ihre Kraft verlieren würden, sollten sie nicht sorgfältig eingesetzt werden. Doch diese Warnungen verflogen im Rausch des medizinischen Erfolgs. Mit jedem neuen Antibiotikum schwand der Respekt vor den einst tödlichen Bakterien, und die Mittel wurden in rauen Mengen verwendet.
Künftig Millionen Tote durch Antibiotikaresistenzen
Mit den Folgen dieser gefährlichen Nachlässigkeit leben wir heute: Allein in Europa infizieren sich jährlich 670 000 Menschen mit Bakterien, gegen die Antibiotika kaum mehr etwas ausrichten. Das Europäische Zentrum für die Überwachung von Infektionskrankheiten (ECDC) schätzt, dass 33 000, also jeder Zwanzigste von ihnen stirbt. Diverse Kalkulationen, so vage sie sein mögen, gehen von einigen Millionen Toten im Jahr 2050 aus.
Das, was Medizinern bis in die 1990er Jahre überflüssig erschien, brauchen sie mittlerweile im drohenden »postantibiotischen Zeitalter«, wie es die Weltgesundheitsorganisation formuliert, umso dringender: Mittel, die nicht alle Bakterien abtöten, sondern nur den einen gefährlichen Keim, den sie zu bekämpfen versuchen – diesen aber effizient. Phagen?
In Tiflis sind derartige Virentherapien längst Alltag. Im Jahr 2011 gründete das Eilava-Institut zu diesem Zweck eigens eine Klinik – vor allem für ausländische Gäste. 3900 Euro kostet die Behandlung gegen einen Standardkeim, 1400 Euro mehr für ausgefallenere Vertreter. Von Tiflis aus haben die Therapien vereinzelt ihren Weg nach Europa und die USA gefunden. Einer der wenigen deutschen Ärzte, die sie einsetzen, ist Burkhardt Wippermann, Chefarzt der Unfallchirurgie am Helios-Klinikum in Hildesheim. Auch er kam über einen georgischen Arzt zu der Behandlung mit den Viren. Nahezu täglich erhält er inzwischen Anfragen von Patienten, denn: »Oftmals funktioniert sie«, sagt Wippermann. Weshalb hat sich die Phagentherapie dann bislang nicht durchgesetzt?
Dilemma der Phagenforschung
»Es fehlt an aussagekräftigen Studien, die zeigen, dass es wirklich funktioniert«, erklärt Martin Witzenrath, stellvertretender Direktor der Klinik für Infektiologie und Pneumologie an der Charité. Der Mediziner forscht in dem vom Bundesforschungsministerium mit vier Millionen Euro geförderten Projekt »phage4cure« an einem inhalierbaren Phagenmix gegen Pseudomonas aeruginosa, das schwere Lungeninfektionen verursacht.
»Haben Sie jemals von einem Fallbericht gelesen, der schiefging?« Zu jedem erfolgreich verlaufenden Einzelfall könnte es davon nämlich hunderte geben. Man wisse nur nichts darüber, weil diese nicht publiziert werden. Um solche Unsicherheiten auszuschließen, bedürfen neue Arzneimittel umfangreicher Tests – zunächst am Tier, später im Gesunden, und schließlich im Kranken. Mit ihrer Hilfe wird die Sicherheit und Wirksamkeit eines jeden Arzneimittels abgeschätzt. Dann erst erlauben die Zulassungsbehörden die Vermarktung. Solche kostengewaltigen Studien übernimmt gewöhnlich die Pharmaindustrie, die später die Mittel vertreibt.
»Die brauchbaren Phagen findet man dort, wo es auch die zu bekämpfenden Bakterien gibt«Christine Rohde
Doch die zeigt bislang wenig Engagement. Denn mit Phagen lässt sich nicht so einfach Geld verdienen. Sie sind natürliche Lebewesen. Solange sie der Umwelt entnommen werden, sind sie keine Erfindungen und lassen sich nicht patentieren. Man muss lediglich wissen, wo man am besten sucht. »Die brauchbaren Phagen findet man dort, wo es auch die zu bekämpfenden Bakterien gibt«, sagt Christine Rohde von der Deutschen Sammlung für Mikroorganismus und Zellkulturen (DSMZ) am Leibniz-Institut in Braunschweig. Und das ist etwa in den Abwässern von Krankenhäusern.
Gemeinsam mit ihrem Team baut Rohde die Phagenbank für »phage4cure« auf. Etwa 800 Phagen haben die Wissenschaftler inzwischen zusammen. Solche, die sie als »potent« erachten, finden ihren Weg weiter ins Fraunhofer Institut für Toxikologie und Experimentelle Medizin (ITEM) in Braunschweig. Dort entwickeln Forscher eine Plattform, mit der aus den Phagen schließlich ein zertifizierte Arzneiprodukt hergestellt werden kann. »Die Reinheit, die Dosierung, die Aufbereitung, die Haltbarkeit der Phagen, – all das muss in genauestens dokumentierten und reproduzierbaren Arbeitsschritten erfolgen«, sagt Rohde. Bekannt ist etwa, dass die Haltbarkeit der Phagen maßgeblich mit der Lösung zusammenhängt, in der sie schwimmen. Salopp ausgedrückt: Je weniger aufgereinigt die Brühe, desto länger überleben die Phagen. Solche Erkenntnisse sind essenziell.
Eine von der EU mitfinanzierte klinische Studie aus dem Jahr 2017, in der Phagen gegen infizierte Brandwunden eingesetzt wurden, scheiterte beispielsweise unter anderem daran, dass etliche davon kaputtgingen. »Es stellte sich heraus, dass die Phagenkonzentration teilweise viel zu gering war«, sagt Rohde.
Nicht nur die Phagen, sondern auch die Lösung, in der sie schwimmen, ist relevant für die Behandlung. Im besten Fall lösen die Inhaltsstoffe sogar eine zusätzliche Abwehrreaktion aus und sorgen dafür, dass die Bakterien bekämpft werden. »Das ist gut für den Patienten, hat aber nichts mit den Phagen zu tun hat«, so der Kliniker Witzenrath. Es kann jedoch durchaus vorkommen, dass die Lösung den Infekt verschlimmert. All diese Punkte sind bisher nicht ausreichend erforscht.
Daher weiß der Spezialist für Infektionskrankheiten Robert »Chip« Schooley im Jahr 2016 nicht, wie sein Patient auf die Phagenbehandlung reagieren wird. Aber es gibt kaum etwas zu verlieren. Also spritzt Schooley eine erste Dosis direkt in den Infektionsherd in der Bauchhöhle. Offenbar wirkt die Behandlung. Schooley geht noch einen Schritt weiter: Intravenös jagt er die Viren durch den Körper seines Patienten. Nach drei Tagen wacht dieser auf. Sechs Monate später verlässt Strathdees Mann die Klinik. Er ist der erste Mensch in den USA, der mit einem Cocktail aus intravenös verabreichten Bakteriophagen erfolgreich von einer systemischen, multiresistenten bakteriellen Infektion geheilt werden konnte.
Phagen machen Antibiotika wieder wirksam
In einer anschließenden Veröffentlichung des Falls, beschreiben Schooley und sein Team, weshalb die Therapie erfolgreich war: Der Kampf gegen die Phagen hätte die gefährlichen Keime teilweise erneut anfällig für bestimmte Antibiotika gemacht. Die »alten Wundermittel« sprachen plötzlich wieder an. Der Fall erregte viel öffentliche Aufmerksamkeit – und weckte Hoffnung bei etlichen Betroffenen.
Nach der fast wundersamen Genesung meldeten sich bei Strathdee Patienten aus aller Welt. Denn erst durch ihre Anstrengungen waren passende Phagen für ihren Mann gefunden worden. Gemeinsam mit Schooley wurde Strathdee daher gewissermaßen zur »Phagenbeauftragten« der USA. Die Suche nach passenden Phagen ging viral, und die vielen Tweets veranlassten zwei Freunde aus den USA, die eine Biologiestudentin, der andere Entwickler, eine Datenbank aufzusetzen, die Phagenforscher und Mediziner weltweit miteinander vernetzt. Auf Phagedirectory können sie nun ihre verfügbaren Phagen eintragen, mitsamt den Bakterien, gegen die sie sich richten. Die Seite hat sich mittlerweile zu einer zentralen Anlaufstelle für die Suche nach Phagen entwickelt.
Um die Anfragen besser zu koordinieren, gründete die University of San Diego 2018 für 1,2 Millionen Dollar ein Center for Phage Applications and Therapeutics (IPATH). Strathdee wurde gemeinsam mit Schooley Kodirektorin. Mindestens fünf Patienten haben sie dort seitdem erfolgreich therapiert.
Mittlerweile gibt es einige Unternehmen, die Phagentherapie entwickeln und kommerziell vermarkten möchten. Der ehemalige Phagenforscher des nationalen US-Gesundheitsinstitut National Health Service (NHS) Carl Merrill hat sich sogar selbst aus dem Ruhestand zurückbeordert, um mit seinem Sohn das Start-up Adaptive Phage Therapeutics (APT) zu gründen. In Strathdees Heimatstadt sammelt das Biotech-Unternehmen Armata finanzielle Unterstützung, um erste Studien zu beantragen, die sowohl Strathdee als auch Schooley dringend fordern. Und in Europa gründete Burkhardt Wippermann, Chefarzt des Helios Klinkum Hildesheim, gemeinsam mit zwei Partnern das Unternehmen PhagoMed. Ihr erklärtes Ziel ist der Aufbau einer Phagenbank mit Exemplaren, die speziell für Therapien gegen bakterielle Infektionen im Vaginal- und Harntrakt eingesetzt werden können. Das ökonomische Dilemma wollen die Unternehmen umgehen, indem sie nicht die Phagen selbst, sondern die Verfahren patentieren lassen, mit deren Hilfe sie die Mikroorganismen sammeln und aufreinigen.
Phagen gentechnisch aufrüsten
Im Jahr 2018 haben britische Ärzte in Zusammenarbeit mit US-Forschern einen Ansatz entwickelt, der die Phagen noch effizienter macht: Sie veränderten die Viren gentechnisch, um ein Mädchen zu behandeln, in deren Lunge sich ein hochresistenter Verwandter des Tuberkuloseerregers eingenistet hatte. Die Patientin vertrug die Therapie gut, und ihr Zustand verbesserte sich, wie die Forscher im Jahr 2019 berichteten.
Im Januar 2020 kündigte das US-Start-up Locus Biosciences eine klinische Studie mit Phagen an, die sich gegen den Harnwegsinfektserreger Escherichia coli richtet. Mit der Genschere CRISPR-Cas3, die gewöhnlich eingesetzt wird, um das Erbgut präzise zu bearbeiten, wollen sie Phagen noch zielgerichteter machen.
Eine gentechnische Veränderung macht die Phagen auch aus finanzieller Perspektive interessanter, da diese Versionen dann patentierbar wären. Und tatsächlich beteiligt sich bei Armata mittlerweile der Pharmakonzern Merck an der Entwicklung synthetischer Phagen. Nur: Bislang gibt es keine rechtlichen Grundlagen, gentechnisch veränderte Phagen zuzulassen.
Aus diesem Grund hat sich ein weiteres Forschungsfeld entwickelt: Die Idee ist, nicht die kompletten Phagen, sondern nur deren zerstörerische Proteine, so genannte Lysine, in den Kampf gegen die Bakterien zu schicken. Sie sollen die Erreger spezifisch erkennen, aufbohren und dadurch unschädlich machen. Neben dem erwähnten Unternehmen Phagomed versucht sich an dieser Methode auch das deutsch-liechtensteinische Unternehmen Lysando.
Unterdessen wurden kürzlich die Ergebnisse einer ersten kleinen Sicherheitsstudie mit Phagen an 13 Patienten an der University of Sydney veröffentlicht. Sie litten an schweren Infektionen mit dem resistenten Staphylokokkus aureus und erhielten einen auf den Erreger abgestimmten Phagenmix von dem US-Unternehmen Armata. Die Studie konnte zeigen, dass die Therapie gut verträglich ist. Die Zahl der Probanden ist aber noch zu klein, um verlässliche Aussagen treffen zu können.
Die deutschen Phagenforscher hoffen, in etwa einem Jahr mit klinischen Studien beginnen zu können. Bei aller Euphorie ob der neuen alten Methode: Witzenrath weiß jedoch auch, dass Phagen ihre Konkurrenten, die Antibiotika, niemals werden ersetzen können. »Aber wir hätten endlich ein weiteres Mittel im Kampf gegen multiresistente Keime«, sagt er.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.