Lexikon der Geowissenschaften: Wasser
Wasser
Hans-Jürgen Liebscher, Koblenz
Wasser mit der chemischen Formel H2O ist einStoff, der durch seine besonderen Eigenschaften (Wasserchemismus) auf der Erde in fester, flüssiger und dampfförmiger Phase sowohl in der Hydrosphäre als auch in der Lithosphäre und in der Atmosphäre existiert. Phasenübergänge erfolgen durch Kondensation, Verdunstung (Verdampfung), Gefrieren, Schmelzen, Sublimation oder Resublimation. In flüssiger Form tritt das Wasser in den Meeren und den Oberflächengewässern des Festlandes auf. Als Boden-, Grund- oder Tiefenwasser durchsetzt es die Lithosphäre und als Wolkenwasser die Atmosphäre. In der festen Form bildet es die Eisschilde der Polargebiete, die Gletscher der Gebirge, die Eisdecken auf den Meeren, Seen und Flüssen sowie die Schneedecken. Eis ist auch in der Atmosphäre und im Boden, zum Beispiel in den Permafrostböden (Permafrost) der höheren Breiten und Gebirgen, zu finden. Wasser ist ferner als Wasserdampf in der Atmosphäre und der Lithosphäre enthalten.
Ohne Wasser ist auf der Erde kein Leben möglich, die Biosphäre würde nicht existieren. Es ist Roh-, Bau- und Betriebsstoff für die Organismen (Wasser in Organismen). Neben Kohlenstoff und Sauerstoff ist es das wichtigste Element zur Bildung von Pflanzenbiomasse. Pflanze, Tier und Mensch bestehen vorwiegend aus Wasser. Es dient als Substanz zur Aufrechterhaltung der Zellstruktur und als Mittel zum Austausch von Stoffen für die Körperfunktionen. Es ist Nahrungsmittel für Pflanzen, Tiere und Menschen. Als Trinkwasser ersetzt es das dem Körper von der meist an Wasserdampf ungesättigten Atmosphäre entzogene Wasser.
Wasser ist in vielen Stoffen gebunden und Lösungsmittel für viele Substanzen. So werden z.B. die Nährstoffe im Boden gelöst und über Saugkräfte im Röhrensystem der Pflanzen zu den Assimilationsorganen geleitet (Transpiration). Wasser ist Hygienemittel, es dient als Reinigungs-, Wasch- und Spülmittel. Es verdünnt oder beseitigt belastende oder giftige Schadstoffe und baut diese ab, sofern sich die Belastung in Grenzen hält (Abbau). Wasser ist Heilmittel und Erholungsmittel für den Menschen, z.B. für den Wasser- und Wintersport oder als Wasserkur. Es ist Lebensraum für aquatische Organismen und damit auch ein Ökosystem. Zudem formt es die Erdoberfläche, z.B. durch Erosion, und es strukturiert die Böden. Wasser ist Transportmittel oder Transportweg im Stoff- und Güteraustausch. Es trägt oder befördert Schiffe und nimmt gelöste oder suspendierte Stoffe im Fließgewässer mit, wie z.B. das Abwasser.
Wasser ist auch Träger von potentieller oder kinetischer Energie. Es wird zur Gewinnung von elektrischer Energie genutzt (Wasserkraftanlage). Es wird ferner zur Übertragung von Energien und Kräften sowie zur Erzeugung hoher Drucke verwendet. Bei Hochwasser wirkt die Kraft des Wassers zerstörend (Naturkatastrophen). Als Rohstoff für die Wirtschaft ist Wasser unentbehrlich. Es dient der Verarbeitung und Synthese von Stoffen, z.B. in Hüttenwerken oder in der Chemieindustrie. Wasser ist ein Kühlmittel in der Natur und in der Technik, z.B. bei thermischer Erzeugung von Energie und bei industriellen Produktionsprozessen. Bei Kühlprozessen wird der Oberfläche durch die Verdunstung Wärme entzogen. Wasser beinhaltet latente Energie, die bei Phasenänderungen durch die Prozesse Verdunstung, Kondensation, Schmelzen, Gefrieren oder Sublimation umgesetzt wird. Es ist somit ein Regler des Energiehaushaltes der Erde und der Wettersysteme in der Atmosphäre. Der Wasserdampftransport sorgt für einen Wasserausgleich auf der Erde.
Im Vergleich zu anderen Stoffen hat das Kontinuum Wasser in mehrfacher Hinsicht anomale Eigenschaften. Dazu gehören vor allem das Dichtemaximum bei 3,98ºC, hohe spezifische Wärme, hoher Siedepunkt, hohe Schmelz- und Verdampfungswärme sowie große Dielektrizitätskonstante. Dies ist durch den Dipolcharakter des Wassers, das kleine Molvolumen und auf die Mischung von verschiedenen Wassermolekülaggregationen im natürlichen Wasser zurückzuführen. Man unterscheidet elektrische, mechanische, optische und thermische Eigenschaften. Alle diese Eigenschaften sind mehr oder weniger stark von der Temperatur und Wasserinhaltsstoffen, besonders vom Salzgehalt abhängig.
Elektrische Eigenschaften
Wasser verfügt, bedingt durch die Molekülstruktur, über Besonderheiten bezüglich der elektrischen Leitfähigkeit für elektrische Ströme und Wellen, Eindringtiefe elektromagnetischer Wellen und der Dielektrizitätskonstante, die sowohl von der Temperatur als auch von den Wasserinhaltsstoffen, insbesondere vom Salzgehalt, beeinflußt werden. Der elektrische Widerstand R ist wegen des geringen Anteils an dissoziierten H+- und an OH--Ionen in reinem Wasser groß und die elektrische Leitfähigkeit k=1/R gering. Letztere liegt bei reinem Wasser je nach Wassertemperatur zwischen 1,6·10-6 und 20·10-6 S/m. In verschmutztem Wasser, z.B. Regenwasser mit niedrigem pH-Wert, steigt die Leitfähigkeit auf ein Vielfaches, z.B. auf 10-4 S/m an. Wasser ist durch eine abnorm hohe Dielektrizitätskonstante gekennzeichnet. Dies ist dadurch bedingt, daß die Wassermoleküle in einem elektrischen Feld versuchen, dieses zu neutralisieren. In einem elektrischen Feld wenden sie ihre negativ geladene Sauerstoffatom-Seite dem Plus-Pol (Anode) und ihre positiv geladene Wasserstoffatom-Seite dem Minus-Pol (Kathode) zu. Die absolute Dielektrizitätskonstante ε0, d.h. für Vakuum, hat den Wert 8,854·10-12 C/(N·m2). Die dimensionslose relative Dielektrizitätszahl (Permittivitätszahl) εr des Wassers mit der Temperatur 20ºC beträgt 80 ( Tab. 1).
Die Eindringtiefe elektromagnetischer Wellen in Wasser ist frequenzabhängig und wird von der Leitfähigkeit der Flüssigkeit mitbestimmt. Die Halbwerttiefe von Längstwellen (VLF, ELF, ULF) beträgt in Frischwasser bei 50 Hz etwa 20 cm, bei 500 Hz 0,5 m, bei 5 kHz 2 m, bei 50 kHz 5 m und für Hochfrequenzwellen (UKW, KW) bei 500 kHz ca. 20 m. Die Eindringtiefe von GHz-Wellen, z.B. Radar, liegt bei über 100 m. In Meerwasser mit hohem Salzgehalt dringen die Wellen erst ab 5 kHz nennenswert ein. Aus der Rückstreuung von Millimeter- und Zentimeter-Wellen lassen sich die Wassergehalte von Schneedecken oder Böden bestimmen (Fernerkundung). Die Strahlungsdurchlässigkeit für UV-Strahlung wird zur Wasserentkeimung ausgenutzt, wobei der Spektralbereich des UVC bei 250-200 nm benutzt wird.
Mechanische Eigenschaften
Wasser hat sowohl im ruhenden als auch im bewegten Zustand besondere mechanische Eigenschaften, die durch Oberflächen- und innere Kräfte bestimmt sind. Diese werden durch die Temperatur ( Tab. 2) und den Salzgehalt beeinflußt. Das spezifische Volumen v des Wassers verringert sich mit abnehmender Temperatur entsprechend der Abnahme der Molekularbewegung, bis sie bei der Temperatur 3,98 ºC mit dem Wert 1,000·10–3 m3/kg ihren kleinsten Wert erreicht hat. Dann aber wird der Einfluß der Wasserstoffbindung stärker als die durch geringere Bewegung der Wassermoleküle bewirkte Zusammenziehung. Die Wassermoleküle beginnen sich entlang der Linien ihrer Wasserstoffbindungen zu ordnen. Dabei bleiben Lücken oder Öffnungen zwischen diesen Linien frei. Das Wasser dehnt sich aus, bis es erstarrt und die Kristallstruktur (Eis) annimmt.
Die Dichte ρ verhält sich invers zum spezifischen Volumen v: ρ=v-1. Beim Gefrieren erfolgt ein Dichtesprung um 9% und führt auf den Wert 0,9168·103 kg/m3 bei 0ºC für reines, luftfreies Eis. Letzteres ist leichter als Wasser; es schwimmt auf diesem und taucht etwa bis zu 90% in das Wasser ein. Das Dichtemaximum bei 3,98ºC bewirkt, daß Gewässer erst dann zufrieren können, wenn das gesamte Wasser auf 3,98ºC abgekühlt ist. Die Dichte des Wassers nimmt mit größer werdendem Salzgehalt zu. Dies ist für das Meerwasser und die Dynamik der Ozeane von besonderer Bedeutung. Wegen des Salzgehaltes gefriert Meerwasser erst unterhalb 0ºC, wodurch sich auch das Dichtemaximum verschiebt. Bei einem Salzgehalt von 2,47% stimmt die Temperatur des Dichtemaximums mit dem Gefrierpunkt von -1,322ºC überein.
Die strenge Wasserstoffbindung im Wassermolekül und im Kontinuum Wasser bewirkt eine ungewöhnliche Kohäsion des Wassers als Flüssigkeit. Dies äußert sich in der hohen Oberflächenspannung. Die molekularen Bindungskräfte verleihen dem Wasser eine Zähigkeit, die bei dessen Strömung zu innerer Reibung oder Viskosität und zu Schubspannungen führen. Der Koeffizient der inneren Reibung η (dynamische Viskosität) hat für Wasser bei 20ºC einen Zahlenwert von etwa 1 mPa·s=10-3 N·s/m2.
Die relative Volumenänderung des Wassers bei einer Druckerhöhung, die Kompressibilität κ, ist außerordentlich klein. Bezogen auf die Druckerhöhung um 1·105 Pa=0,1·106 N/m2 beträgt die relative Volumenänderung nur 10-9 hPa-1. Die Relaxationszeit τ, d.h. die Einstellzeit nach Formveränderungen auf (1/e)=0,368 des Anfangszustandes, ist extrem kurz und sie liegt in der Größenordnung von 10-11 bis 10-13 Sekunden. Die Ausbreitungsgeschwindigkeit vs von Schallwellen im Wasser hängt von der Dichte und der Kompressibilität ab. Sie beträgt bei reinem Wasser von 25ºC etwa 1500 m/s. Im Meerwasser mit 3,5% Salzgehalt laufen die Schallwellen langsamer, und zwar mit 1450 m/s. Die Schallgeschwindigkeit wird zur Tiefenlotung oder zur Messung der Fließgeschwindigkeit genutzt (Durchflußmessung). Sie wächst mit steigender Temperatur.
Optische Eigenschaften
Hydrologisch bedeutsame optische Eigenschaften des Wassers sind die Strahlungsreflexion an der Wasseroberfläche, die Lichtbrechung an der Grenzfläche Wasser/Luft, die Strahlungstransmission und die Strahlungsstreuung im Wasser. Diese Eigenschaften werden von Trübstoffen im Wasser beeinflußt. Die Strahlungsreflexion R ist sowohl von der Wellenlänge als auch von der Einfallsrichtung der Strahlung abhängig. Sie wird nach der Gleichung von Fresnel beschrieben:
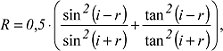
wobei i den Einfallswinkel der Strahlung (z.B. Sonnenhöhe) und r den Brechungswinkel darstellen. Wasseroberflächen reflektieren im Lichtwellenbereich (λ=0,4-0,7 μm) etwa 5-7%. Sie absorbieren die Infrarotstrahlung (λ=3 μm) schon in dünnen Wasserschichten nahezu vollständig. Die integrierte Reflexion über alle Wellenlängen, die Albedo, beträgt für solare Strahlung (0,38-3 μm) 6-12%, für die Lichtwellen (0,4-0,76 μm) 5-15 % und für die terrestrische Strahlung (3-100 μm) etwa 4,5%.
Die Lichtbrechung an der Grenze Wasser/Luft ist durch eine Strahlkrümmung zum optisch dichteren Medium hin, dem Wasser, gekennzeichnet. Sie wird durch den Refraktionsindex:
n1,2=sinα/sinβ=1,333
beschrieben, wobei n1,2 zur Luft=1,00029 und der Einfallswinkel mit der Sonnenhöhe gleich gesetzt werden kann. Beim Erreichen des Grenzwinkels von αg=βg=48,5º wird das Licht in das Wasser hineingebrochen. Unterlicht, das vom Wasser her zur Oberfläche weist, unterliegt der Totalreflexion. Die Brechzahl von Eis beträgt 1,31.
Wasser ist für die Strahlung durchlässig. Mit zunehmender Tiefe wird die Intensität durch Absorption und Streuung gedämpft. Die Schwächung oder Extinktion kann durch das Lambert-Beersche Gesetz beschrieben werden. Dabei hängt die Strahlungsintensität I im Wasser in der Tiefe z von der Strahlungsdichte Io an der Wasseroberfläche und vom Extinktions- oder Absorptionskoeffizient a ab:
I=I0·e-a·z.
Diese Gleichung gilt für homogene Medien sowohl für monochromatische als auch für die Gesamtstrahlung. Die Durchlässigkeit D einer Wasserschicht d folgt aus:
D=(Id/Io)d.
Dabei stellt das Verhältnis Id/Io den Transmissionsfaktor dar. Die Transmission T ergibt sich zu:
T=Io-I.
Der Absorptionskoeffizient a ist eine Funktion der optischen Eigenschaften des reinen Wassers und seiner gelösten kolloidalen und partikularen Inhaltsstoffe wie mineralische Schwebstoffe oder Organismen, z.B. Algen.
Die Lichtstreuung oder innere Reflexion im Wasser ist ebenfalls wellenlängenabhängig von Grad und Art der Trübung bestimmt. Die Trübung bestimmt die Sichttiefe. Sie ist die gemeinsame Wirkung von Streuung und Absorption und nimmt mit steigendem Feststoffgehalt ab. Der Trübungsfaktor T gibt an, wie viele Schichten reinen Wassers benötigt werden, um die gleiche Extinktion wie bei verunreinigtem Wasser zu erzeugen. Die Lichtstreuung erzeugt das Unterlicht, das bei flachen Gewässern auch durch die Reflexion am Gewässergrund verstärkt wird. Auf der Streuung beruht die Wasserfarbe. Reines Wasser erscheint blau. Feinste Mineralstoffe erzeugen grüne, grobes Mineral graue Farbtöne. Ton und humose Stoffe geben dem Wasser gelbe, braune bis schwarze Farbe.
Thermische Eigenschaften
Mit der Wasserstoffbindung der Wassermoleküle sind auch die besonderen thermischen Eigenschaften von Wasser verbunden. Diesesind sowohl für Wasser in gasförmiger, flüssiger und fester Form temperatur- und druckabhängig. Die Aggregatzustände sind durch den Gefrier- oder Schmelzpunkt und durch den Siede- oder Kondensationspunkt getrennt. Im Tripelpunkt bei 0,0098ºC und 6,11 hPa Dampfdruck können alle Zustandsformen permanent nebeneinander bestehen. Die Phasenübergänge durch Kondensation, Verdunstung, Gefrieren, Schmelzen, Sublimation und Eisverdampfung sind mit Energieumsätzen verbunden. Dabei sind die Phasenübergänge Eis-Wasser-Eis von erheblich geringeren Energieumsätzen begleitet als bei den Aggregatsänderungen Wasser-Dampf-Wasser oder Dampf-Eis-Dampf.
Die spezifische Wärme von Wasser cw ist im Vergleich zu anderen Flüssigkeiten sehr hoch ( Tab. 3). Die Abhängigkeit von der Temperatur T wird durch:
cw=4,21-0,00177·T+0,0000127·T2
beschrieben. Sie wächst auch mit steigendem Salzgehalt. Wasser ist auch durch eine große Volumenwärmekapazität c·ρ gekennzeichnet. Der Wärmeinhalt, die Enthalpie ε, steigt mit der Temperatur. Sowohl die spezifische Wärme als auch die Wärmekapazität bewirken die bedeutende Rolle des Wassers im Wärmehaushalt der Atmosphäre und der Grenzschicht Erdoberfläche/Atmosphäre. Die spezifische Wärme der Luft beträgt je nach Luftfeuchte nur 0,71-1,0·103 J/(kg·K) und die Wärmekapazität der Luft nur 1,3·J/(m·K). Wasser ist bei gleicher Temperatur viel energiereicher.
Auch die molekulare Wärmeleitfähigkeit λ ist von der Temperatur abhängig. Im unbewegten oder laminar fließenden Wasser beträgt sie 0,6 W/(m·K) bei 20ºC. Die Temperaturleitfähigkeit k des unbewegten Wassers:
k=λ/(c·ρ)
nimmt wegen der hohen Wärmekapazität c·ρ nur 1/100 der Werte der Luft an und zwar 0,15·10-6 m2/s.
Die spezifische Wärme von Eis ce ist nur etwa halb so groß wie jene von flüssigem Wasser, und zwar beträgt sie bei 0ºC 2,11·103 J/(kg·K). Die Molwärme liegt bei 38,5 J/(mol·K). Entsprechend der geringen spezifischen Wärme sowie wegen des Dichtesprunges bei 0ºC ist die Wärmekapazität nur 47% jener von flüssigem Wasser, und zwar bei –20ºC von der Größe 1,80·106 J/(m3·K) und bei 0ºC 1,93·106 J/(m3·K). Die Wärmeleitfähigkeit von Eis ist wesentlich höher als die von Wasser. Bei 0ºC beträgt sie 22,2 W/(m·K) und ist damit vier mal größer. Die Wärmeleitzahlen sind abhängig von der Schneedichte. Für Neuschnee beträgt die Wärmeleitzahl 0,08 W/(m·K) und für Altschnee ca. 1,5 W/(m·K). Neuschnee ist ein besonders guter Wärmeisolator. Die Temperaturleitzahl liegt nur bei etwa 0,5·10-6 m2/s und ist etwa vier mal größer als jene von Wasser.
Wasser (Tab. 1): elektrische Eigenschaften von reinem Wasser als Funktion der Temperatur T (εr=relative Dielektrizitätskonstante, k=elektrische Leitfähigkeit). Wasser (Tab. 1):

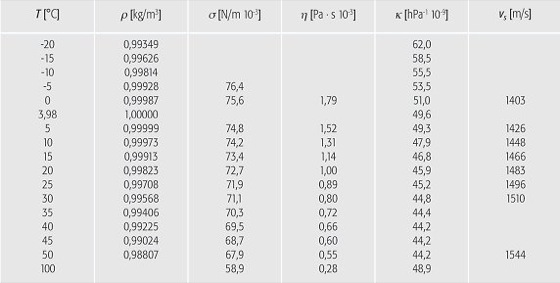
Wasser (Tab. 2): mechanische Eigenschaften des Wassers in Abhängigkeit von der Temperatur T (ρ=Dichte, σ=Oberflächenspannung, η=absolute (dynamische) Viskosität, κ=Kompressibilität, vs=Schallgeschwindigkeit bei 750 kHz in destilliertem Wasser). Wasser (Tab. 2):
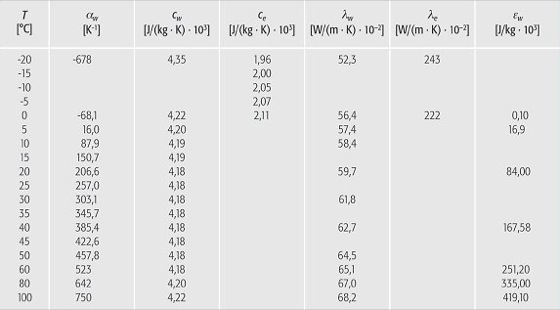
Wasser (Tab. 3): Kenngrößen zur Thermodynamik des Wassers in Abhängigkeit von der Temperatur T (α=thermische Ausdehnung, c=spezifische Wärme, λ=Wärmeleitfähigkeit, ε=Enthalpie; mit den Indizes w für Wasser und e für Eis). Wasser (Tab. 3):
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.